题目内容
1.有些酸随着浓度的改变会表现出不同的化学性质.请回答下列问题:(1)用毛笔蘸取稀硫酸在竹叶上画花,然后把竹叶放在小火上烘干,再用水洗净,在竹片上就得到一幅精美的呈黑色或褐色的竹片画.在烘干的过程中稀硫酸变为浓硫酸,在制作竹片画的过程中利用了浓硫酸的脱水性.
(2)在加热的条件下浓硫酸与铜反应的方程式是Cu+2H2SO4(浓)$\frac{\underline{\;△\;}}{\;}$CuSO4+SO2↑+2H2O.但足量的铜和浓硫酸充分反应后溶液中仍有少量硫酸剩余,其原因是铜与浓硫酸反应生成水,浓硫酸变成稀硫酸,而铜与稀硫酸不反应,故反应后溶液中仍有硫酸剩余.
分析 (1)浓硫酸具有脱水性;
(2)铜与浓硫酸反应生成水,浓硫酸变成稀硫酸,而铜与稀硫酸不反应,所以足量的铜和浓硫酸充分反应后溶液中仍有硫酸剩余.
解答 解:(1)稀硫酸在烘干的过程中水分不断蒸发逐渐变为浓硫酸,浓硫酸具有脱水性能将竹片中的氢、氧元素按水的比例析出从而使竹片碳化变黑;
故填:脱水;
(2)铜与浓硫酸反应生成水,浓硫酸变成稀硫酸,而铜与稀硫酸不反应,所以足量的铜和浓硫酸充分反应后溶液中仍有硫酸剩余.
故填:铜与浓硫酸反应生成水,浓硫酸变成稀硫酸,而铜与稀硫酸不反应,故反应后溶液中仍有硫酸剩余.
点评 本题主要考查浓硫酸和稀硫酸的性质,难度不大.

练习册系列答案
相关题目
14.下列各组现象属于化学变化的是( )
| A. | 蜡烛熔化 | B. | 铁锅生锈 | C. | 电灯发光 | D. | 汽油挥发 |
14.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定的条件下,充分反应,测得反应前后各物质质量如下表
关于此反应,下列认识正确的是( )
| 物 质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 5 | 2 | 42 | 12 |
| 反应后质量(g) | X | 2 | 6 | 40 |
| A. | 乙一定是催化剂 | |
| B. | 参加反应的丙、丁的质量比为1:2 | |
| C. | X的值为13 | |
| D. | 乙、丙中所含元素种类与甲、丁中所含元素种类相同 |
16.下列实验装置或操作,能达到相应实验目的是( )
| A. |  干燥氢气 | B. |  验证Zn、Fe、Cu的活动性强弱 | ||
| C. |  氢气还原氧化铜 | D. |  检验X溶液中是否含有SO42- |
13.下列各组物质按单质、化合物、混合物的顺序排列的是( )
| A. | 矿泉水、氧化镁、空气 | B. | 氮气、过氧化氢、氯酸钾 | ||
| C. | 木炭、水银、牛奶 | D. | 金刚石、冰水、牛奶 |
10.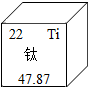 钛和钛合金是21世纪的重要材料,具有很多优良性能,钛元素在化合物中一般显+4价,它在元素周期表中的部分信息见图,下列说法中错误的是( )
钛和钛合金是21世纪的重要材料,具有很多优良性能,钛元素在化合物中一般显+4价,它在元素周期表中的部分信息见图,下列说法中错误的是( )
 钛和钛合金是21世纪的重要材料,具有很多优良性能,钛元素在化合物中一般显+4价,它在元素周期表中的部分信息见图,下列说法中错误的是( )
钛和钛合金是21世纪的重要材料,具有很多优良性能,钛元素在化合物中一般显+4价,它在元素周期表中的部分信息见图,下列说法中错误的是( )| A. | 钛元素原子的质子数为22 | B. | 钛元素的相对原子质量为47.87 | ||
| C. | 钛元素属于非金属元素 | D. | 钛原子核外共有22个电子 |