题目内容
1.在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应的认识不正确的是( )| 物质 | M | N | Q | P |
| 反应前质量(g) | 18 | 1 | 2 | 32 |
| 反应后质量(g) | X | 26 | 2 | 12 |
| A. | 反应后物质M的质量为13g | B. | 反应中N、P的质量比为5:4 | ||
| C. | 物质Q一定是该反应的催化剂 | D. | 该反应属于化合反应 |
分析 根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.反应后质量增加的是生成物,减少的是反应物,由表格信息可知反应后M质量是13克,是反应物;N质量增加了25克,是生成物;Q质量不变,可能是催化剂,P质量减少了20克,是反应物;所以推断:Q质量不变,可能是催化剂,反应物是M和P,生成物是N,所以是化合反应,反应中N和P的质量比为25:20=5:4.
解答 解:反应前后质量不变,所以18+1+2+32=X+26+2+12,x=13g
M、P质量都减少,N增加,M反应掉了18g-13g=5g.P的反应质量为32g-12g=20g.生成的N的质量为26g-1g=25g.数据可以如此处理,如下:
| 物质 | M | N | Q | P |
| 反应前质量(g) | 18 | 1 | 2 | 32 |
| 反应后质量(g) | X=13 | 26 | 2 | 12 |
| 质量变化 | -5 | +25 | 0 | -20 |
B、反应中N、P的质量比为:25g:20g=5:4.正确;
C、物质Q的质量在反应前后不变,可能是该反应的催化剂.错误;
D、反应物是两种,生成物是一种,属于化合反应.正确.
故选:C.
点评 在化学反应中遵循质量守恒定律,参加反应的物质的质量等于反应后生成的物质的质量.解此题需认真分析各物质的质量变化情况,仔细推敲,即可求解.

练习册系列答案
相关题目
9.下列有关16号元素硫(S)的说法不正确的是( )
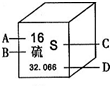

| A. | 该元素原子的质子数为16 | B. | 该元素的相对原子质量为32.066克 | ||
| C. | 该元素原子的原子序数为16 | D. | 该元素为非金属元素 |
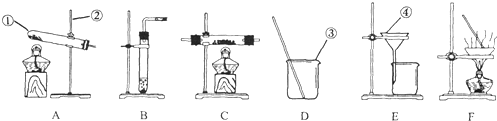
16.掌握正确的操作是做好化学实验的基础,下列实验操作错误的是( )
| A. | 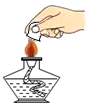 盖灭酒精灯 | B. | 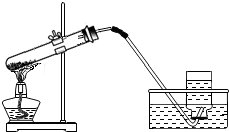 实验室制氧气 | ||
| C. | 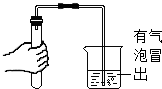 检查装置气密性 | D. | 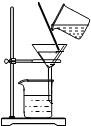 过滤液体 |
6.卢瑟福在测定原子构成时做了如下实验:用α粒子(带正电荷)轰击一极薄的金箔,结果发现大多数粒子通过了金箔,只有极少数发生了偏转或被弹回.根此得出的结论中,正确的是( )
| A. | 金原子是实心球体,紧密结合排列 | |
| B. | 金原子带正电荷 | |
| C. | 相对于金原子而言,金原子核体积很小 | |
| D. | 金原子的质量主要集中在原子核上 |
13.有一包白色固体样品,可能是碳酸钠、硫酸钡、氢氧化钠、氯化钡中的一种或几种.为探究其成分,小燕老师取用一定量样品,加足量水溶解,过滤得到白色沉淀甲和无色滤液乙.
写出上述操作中可能发生反应的化学方程式:BaCl2+Na2CO3=BaCO3↓+2NaCl.
过滤时用到玻璃棒,玻璃棒的作用是引流.
【探究活动一】奋进小组探究白色沉淀甲的成分.
【探究活动二】智慧小组探究白色固体样品中可能含有NaOH,设计了如下实验.
【反思】实验Ⅱ中步骤①加入过量试剂的目的是除去滤液中的Na2CO3,排除干扰.
【结论】通过两个小组的共同探究,得出了原白色固体样品含有的成分.
写出上述操作中可能发生反应的化学方程式:BaCl2+Na2CO3=BaCO3↓+2NaCl.
过滤时用到玻璃棒,玻璃棒的作用是引流.
【探究活动一】奋进小组探究白色沉淀甲的成分.
| 实验操作 | 实验现象 | 结 论 |
| 取白色沉淀甲,滴加足量的稀硝酸 | 沉淀部分消失 | 白色沉淀甲中一定含有BaCO3和BaSO4 |
| 实验操作 | 实验现象 | 结论 | |
| 实验Ⅰ | 取适量无色滤液乙,加入碳酸钠溶液 | 无明显现象 | 无色滤液乙中一定不含BaCl2 |
| 实验Ⅱ | 步骤①:取适量无色滤液乙,加入过量的BaCl2溶液,过滤 | 生成白色沉淀 | 原白色固体样品中一定存在该物质 |
| 步骤②:取步骤①中的滤液,滴加无色酚酞溶液 | 酚酞溶液变红 | ||
【结论】通过两个小组的共同探究,得出了原白色固体样品含有的成分.
10.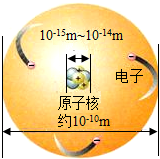 原子的构成示意图如图,下列叙述正确的是( )
原子的构成示意图如图,下列叙述正确的是( )
 原子的构成示意图如图,下列叙述正确的是( )
原子的构成示意图如图,下列叙述正确的是( )| A. | 原子是实心球体 | |
| B. | 整个原子的质量主要集中在原子核上 | |
| C. | 原子、中子、电子均匀分布在原子中 | |
| D. | 质子与电子质量相等 |
20.将Fe、Cu、X三种金属片分别放人稀硫酸中,只有Fe、X表面有气泡;把Fe加入X的硫酸盐溶液中,Fe的表面析出X.则下列说法正确的是( )
| A. | 3种金属的活动顺序为:X>Fe>Cu | |
| B. | 将X加入CuSO4,溶液中无Cu析出 | |
| C. | 将Fe加入CuSO4溶液中,溶液质量一定增加 | |
| D. | 若X的常见价态为+2价,则下列反应不能实现:X+MgS04=XS04+Mg |