题目内容
8.材料是人类赖以生存和发展的重要物质,目前使用量最多的金属材料仍然是钢铁
(一)铁材料的有关知识
1.人类使用金属先后经历了“青铜”、“铁器”时代,直到近代才开始大量使用铝材料.
这也反映出Cu、Fe、Al三种金属的活动性由强到弱的顺序是Al、Fe、Cu.
2.钢铁材料通常分为生铁和钢.如图1是我国1997年发行的纪念钢产量首次突破1亿吨的邮票.邮票通常密封保存在聚乙烯塑料袋中
①以上叙述中不涉及到的材料是B(选填序号).
A.合金 B.无机非金属材料 C.有机合成材料
②以赤铁矿为原料冶炼铁反应的化学方程式
③钢铁露置在空气中易生锈,请提出防止其生锈的一种措施涂油.
(二)铁及其化合物的实验
1.将Fe粉溶于稀H2SO4,此反应属于置换反应(填基本反应类型).用点燃法检验生成的H2前必须验纯.
2.向上述反应后的溶液中滴加NaOH溶液,生成白色Fe(OH)2沉淀,随后沉淀变为灰绿色.
①生成Fe(OH)2反应的化学方程式2NaOH+FeSO4=Fe(OH)2↓+Na2SO4.
②白色沉淀变为灰绿色的原因之一是部分Fe(OH)2接触空气生成Fe(OH)3,反应的化学方程式4Fe(OH)2+O2+2H2O=4Fe(OH)3.生成的Fe(OH)3分解为Fe2O3.
③过滤、洗涤、低温干燥得到灰绿色固体,其组成为2FeSO4•2Fe(OH)2•Fe2O3〔相对分子质量为644].能证明固体已洗净的方法为取少量洗涤液于试管中,滴加氢氧化钠溶液,没有明显变化.
(三)灰绿色固体的热分解实验
兴趣小组称取此固体6.44g,在科研人员的指导下用如图2装置进行热分解实验.
[查阅资料]
①Fe(OH)2在150℃~200℃时完全分解为FeO;
②FeSO4在450℃~500℃时完全分解为Fe2O3,2FeSO4$\frac{\underline{\;450℃~500℃\;}}{\;}$Fe2O3+SO2↑+SO3↑.
1.加热前后及过程中均通入N2,加热前通N2的目的是将装置内的空气赶出.
2.控制温度在不同的范围对A中样品加热,测得剩余固体质量随温度的变化如图3所示.B装置中浓硫酸只能吸收SO3和H2O,当加热到t1℃时,装置C中的现象为紫红色的溶液颜色慢慢变浅.
①图3中E点对应的m1=6.08g.
②图3中F点对应物质中Fe2O3的质量为3.2g.
③科研人员将F点所得剩余固体隔绝空气,在密闭容器中加热到1400℃,得到纯净的磁性Fe3O4.已知加热过程中发生两个反应,且反应前后固体总质量不变.请写出其中一个反应的化学方程式Fe2O3+FeO$\frac{\underline{\;高温\;}}{\;}$Fe3O4.
分析 (一)根据金属的活动性来分析;根据材料的分类来分析;首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.根据生锈的条件考虑防锈的措施;
(二)根据金属的化学性质以及反应类型的判断、氢气的验纯来分析;根据反应的原理来书写方程式;根据亚铁离子的检验方法来分析;
(三)根据加热前装置内有空气来分析;根据高锰酸钾具有氧化性来分析;根据2FeSO4•2Fe(OH)2•Fe2O3中的氢氧化亚铁分解为FeO来分析;根据FeSO4的质量来计算Fe2O3的质量;根据题干信息来分析解答.
解答 解:(一)1、Cu、Fe、Al三种金属的活动性由强到弱的顺序是Al、Fe、Cu;故填:Al、Fe、Cu;
2、①钢和生铁属于金属材料、聚乙烯塑料属于有机合成材料,不包括无机非金属材料;故填:B;
②用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
③铁生锈的条件是与氧气和水共同接触,只要将铁制品与水或氧气隔绝就行了,所以在铁制品表面涂油、喷漆即可;故填:涂油(答案合理即可);
(二)1、铁与稀硫酸反应生成硫酸亚铁和氢气,是由一种单质与一种化合物反应生成新的单质与新的化合物,属于置换反应,氢气具有可燃性,若不纯点燃可能会发生爆炸,所以点燃氢气之前,一定要验纯;故填:置换反应;验纯;
2、①硫酸亚铁与氢氧化钠发生复分解反应生成氢氧化亚铁和硫酸钠;故填:2NaOH+FeSO4=Fe(OH)2↓+Na2SO4;
②氢氧化亚铁、水与氧气反应生成氢氧化铁;故填:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
③若没有洗净则洗涤液中含有亚铁离子,可取少量洗涤液于试管中,滴加氢氧化钠溶液,若出现白色沉淀则没有洗净,否则就洗净了;故填:取少量洗涤液于试管中,滴加氢氧化钠溶液,没有明显变化;
(三)1、加热前,通入一段时间N2的目的是将装置内的空气赶出,防止氢氧化亚铁氧化为氢氧化铁;故填:将装置内的空气赶出;
2、高锰酸钾具有氧化性,能吸收二氧化硫,溶液由紫红色变浅,故填:紫红色的溶液颜色慢慢变浅;
①图3中E点对应的m1为2FeSO4•2Fe(OH)2•Fe2O3中的氢氧化亚铁分解为FeO后剩余固体的质量,设生成水的质量为x
2FeSO4•2Fe(OH)2•Fe2O3--2H2O
644 36
6.44g x
$\frac{644}{36}=\frac{6.44g}{x}$
x=0.36g
则m1=6.44g-0.36g=6.08g;故填:6.08;
②设生成Fe2O3的质量为y,
6.44g2FeSO4•2Fe(OH)2•Fe2O3中含有FeSO4的质量为:6.44g×$\frac{152×2}{644}×100%$=3.04g
6.44g2FeSO4•2Fe(OH)2•Fe2O3中含有Fe2O3的质量为:6.44g×$\frac{160}{644}×100%$=1.6g
2FeSO4$\frac{\underline{\;450℃~500℃\;}}{\;}$Fe2O3+SO2↑+SO3↑
304 160
3.04g y
$\frac{304}{160}=\frac{3.04g}{y}$
图3中F点对应物质中Fe2O3的质量为1.6g+1.6g=3.2g;故填:3.2;
③氧化铁与氧化亚铁在高温的条件下反应生成了四氧化三铁;故填:Fe2O3+FeO$\frac{\underline{\;高温\;}}{\;}$Fe3O4.
点评 本题综合考查了金属的活动性、材料的分类、金属的冶炼、金属的防锈、物质的制备,具有一定的难度,解答时要根据所学知识、结合题干信息认真分析解答.

| A化学与生活 | B化学与环境 |
| ①用灼烧的方法能鉴别尼龙线和羊毛线 ②利用活性炭的吸附性来净化水 ③用熔点低的武德合金做保险丝 | ①酸雨主要是由CO2、SO2气体引起的 ②PM2.5是造成雾霾天气的“元凶”之一 ③大量施用化肥促进农作物的生长 |
| C化学与健康 | D化学与安全 |
| ①发霉的谷物晾晒后即可食用 ②酱油加铁预防缺铁性贫血 ③加入肥皂水降低饮用水的硬度 | ①酒精洒在桌上不慎燃烧起来,可以用水浇灭 ②误服重金属盐溶液,可以喝鸡蛋清或牛奶解毒 ③大量燃放烟花鞭炮增添节日气氛 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 氧气用于医疗急救 | B. | 二氧化碳灭火 | ||
| C. | 熟石灰改良酸性土壤 | D. | 用铜作导线 |
| A. | 氧化物中都含有氧元素,所以含氧元素的化合物一定是氧化物 | |
| B. | 饱和溶液不能继续溶解某种溶质,则饱和溶液也不能继续溶解其他溶质 | |
| C. | NaOH溶液中的OH-能与酸反应,则KOH溶液中的OH-也能与酸反应 | |
| D. | 盐是由金属离子和酸根离子构成的,NH4NO3中没有金属离子,不属于盐 |
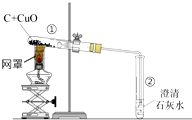 用木炭还原氧化铜的实验如图.
用木炭还原氧化铜的实验如图. A、B、C、D、E均为初中化学常见的化合物.其中A、B、C均含同一种金属元素,C可用于改良酸性土壤,D的溶液呈蓝色,E是一种常见的酸.它们之间存在如图所示的转化关系(“一”表示相互间能反应,“→”表示在某种条件下能生成该物质,部分反应物和生成物已略去). 请回答下列问题.
A、B、C、D、E均为初中化学常见的化合物.其中A、B、C均含同一种金属元素,C可用于改良酸性土壤,D的溶液呈蓝色,E是一种常见的酸.它们之间存在如图所示的转化关系(“一”表示相互间能反应,“→”表示在某种条件下能生成该物质,部分反应物和生成物已略去). 请回答下列问题.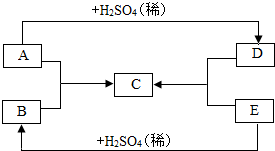 A、B、C、D为初中化学常是的物质,它们之间存在如下图所示的转化关系.已知
A、B、C、D为初中化学常是的物质,它们之间存在如下图所示的转化关系.已知