题目内容
5. 在宏观、微观、符号之间建立联系是化学特有的思维方式.在稀盐酸中加入过量锌粒制取氢气的实验中:
在宏观、微观、符号之间建立联系是化学特有的思维方式.在稀盐酸中加入过量锌粒制取氢气的实验中:(1)宏观表征:可以观察到的主要现象为生成大量气泡,固体逐渐溶解变小.
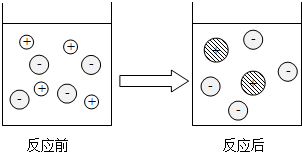
(2)微观表征:右图表示反应前后溶液中的主要离子,写出每种图表示的离子编号:①H+ ②Zn2+ ③Cl-
 ①
① ③
③ ②
②(3)符号表征:写出反应方程式Zn+2HCl═ZnCl2+H2↑.
分析 (1)根据锌与盐酸的反应分析回答现象;
(2)根据反应前后溶液中存在的离子分析;
(3)根据锌与盐酸的反应写出反应的化学方程式.
解答 解:(1)在稀盐酸中加入过量锌粒,生成了氢气和氯化锌,所以,可以观察到的主要现象为:生成大量气泡,固体逐渐溶解变小.
(2)在稀盐酸中加入过量锌粒,生成了氢气和氯化锌,在反应前的溶液中存在氢离子和氯离子,在反应的溶液中存在氯离子和锌离子,由反应前后溶液中存在微粒的示意图可知,每种图表示的离子编号 应为氢离子,
应为氢离子, 为氯离子,
为氯离子, 为锌离子;
为锌离子;
(3)在稀盐酸中加入过量锌粒,生成了氢气和氯化锌,反应方程式为:Zn+2HCl═ZnCl2+H2↑.
故答为:(1)生成大量气泡;(2)①③②;(3)Zn+2HCl═ZnCl2+H2↑.
点评 本题的难度不大,了解锌与盐酸反应前后溶液溶液中离子的变化是解答本题的基础.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15. 某化学实验室产生的废液中含有FeCl3、CuCl2、BaCl2三种物质,现设计下列方案对废液进行处理,以回收金属并制备氯化钡、氯化铁晶体下列说法不正确的是( )
某化学实验室产生的废液中含有FeCl3、CuCl2、BaCl2三种物质,现设计下列方案对废液进行处理,以回收金属并制备氯化钡、氯化铁晶体下列说法不正确的是( )
 某化学实验室产生的废液中含有FeCl3、CuCl2、BaCl2三种物质,现设计下列方案对废液进行处理,以回收金属并制备氯化钡、氯化铁晶体下列说法不正确的是( )
某化学实验室产生的废液中含有FeCl3、CuCl2、BaCl2三种物质,现设计下列方案对废液进行处理,以回收金属并制备氯化钡、氯化铁晶体下列说法不正确的是( )| A. | 沉淀1中的单质为铁和铜 | |
| B. | 氧化方程式为2FeCl2+H2O2+2HCl═2FeCl3+2 H2O | |
| C. | “过滤3”到“氧化”是为了充分回收铁元素 | |
| D. | 试剂X应为NaOH |
16.在研究性学习中同学们了解到氢气具有还原性.他们用氢气还原氧化铜的方法测定某氧化铜样品的纯度(杂质不与氢气反应),同学们设计了以下实验装置,准确称取15克干燥样品进行实验.

(1)在实验中,乙装置的作用是检验水是否除尽;
(2)准确称取完全反应前后装置丙和丁的质量如表:
甲同学想根据装置丁的质量变化进行计算,请帮甲同学求出氧化铜样品的纯度(写出计算过程).
乙同学根据装置丙减少的质量就是氧元素质量,求得氧化铜的质量为11.5克,纯度为76.7%.
(3)比较两种计算结果,请分析导致这一结果的原因可能是
A.装置的气密性不好 B.空气中的水分被丁处浓硫酸吸收
C.通入的氢气量不足 D.空气中的二氧化碳被丁处浓硫酸吸收.
在针对这一结果,对实验装置提出你的一条改进建议在丁的后面增加一个盛有碱石灰的干燥管.

(1)在实验中,乙装置的作用是检验水是否除尽;
(2)准确称取完全反应前后装置丙和丁的质量如表:
| 装置丙 | 装置丁 | |
| 反应前 | 48.8克 | 161.2克 |
| 反应后 | 46.5克 | 163.9克 |
乙同学根据装置丙减少的质量就是氧元素质量,求得氧化铜的质量为11.5克,纯度为76.7%.
(3)比较两种计算结果,请分析导致这一结果的原因可能是
A.装置的气密性不好 B.空气中的水分被丁处浓硫酸吸收
C.通入的氢气量不足 D.空气中的二氧化碳被丁处浓硫酸吸收.
在针对这一结果,对实验装置提出你的一条改进建议在丁的后面增加一个盛有碱石灰的干燥管.
13.陶瓷刀使用纳米氧化锆 陶瓷高压制成,锋利度是钢刀的十倍以上,纳米氧化锆陶瓷属于( )
| A. | 复合材料 | B. | 无机金属材料 | C. | 合成材料 | D. | 无机非金属材料 |
20.蛋白质是人体必需的营养物质,它在人体内最终分解为( )
| A. | 葡萄糖 | B. | 维生素 | C. | 脂肪酸 | D. | 氨基酸 |
17.下列涉及学科观点的有关说法正确的是( )
| A. | 微粒观: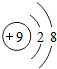 和 和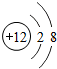 两个粒子核外电子数相同,属于同种元素 两个粒子核外电子数相同,属于同种元素 | |
| B. | 转化观:任何不饱和溶液降低温度后,一定会转化为饱和溶液 | |
| C. | 能量观:硝酸铵固体溶于水放出热量,天然气燃烧吸收热量 | |
| D. | 结构观:金刚石和石墨物理性质存在较大差异是由于碳原子排列方式不同 |
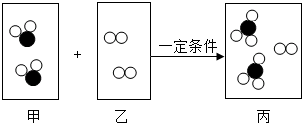
14.图为某化学反应的微观示意图,图中“ ”表示硫原子,“
”表示硫原子,“ ”表示氧原子.下列说法中错误的是( )
”表示氧原子.下列说法中错误的是( )
 ”表示硫原子,“
”表示硫原子,“ ”表示氧原子.下列说法中错误的是( )
”表示氧原子.下列说法中错误的是( )
| A. | 该反应属于化合反应 | |
| B. | 反应前后硫元素的化合价发生了改变 | |
| C. | 反应中甲、乙两物质的质量之比为2:1 | |
| D. | 反应中甲、乙、丙三种物质的化学计量数之比为2:1:2 |
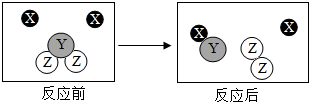 如图是某化学变化的微观示意图,X、Y、Z分别表示不同类别的原子,据图回答问题:
如图是某化学变化的微观示意图,X、Y、Z分别表示不同类别的原子,据图回答问题: