题目内容
1.实验室常用的干燥剂碱石灰是CaO和NaOH的固体混合物,极易与空气中的水蒸气和二氧化碳反应而变质.某同学对一瓶久置的碱石灰作了如下探究:【提出猜想】猜想一:没有变质,只有CaO和NaOH两种固体;
猜想二:已完全变质,碱石灰全部变成了CaCO3和Na2CO3.
【实验探究】实验过程与现象如图所示:
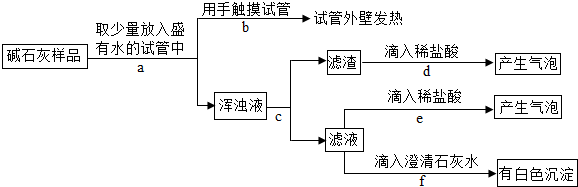
【做出判断】
(1)若把Ca(OH)2、CaCO3和Na2CO3加入水中不会放出热量,侧由操作b中的现象可判断猜想二不成立(填“成立”或“不成立”).
(2)操作f中发生反应的化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;由操作e、f中的现象可判断滤液里含有Na2CO3(填化学式),由此判断猜想一不成立(填“成立”或“不成立”).
(3)综合(1)、(2)中的结论,判断该碱石灰的变质情况为部分变质.
【拓展应用】
(4)由上述实验说明,在实验室存放碱石灰应密封保存.操作c中玻棒的作用是引流.
分析 (1)根据物质溶于水的温度变化情况进行分析,
(2)根据推导确定混合物的成分进行分析,
(3)根据实验现象进行分析,
(4)根据上面的实验结论进行分析,根据过滤操作中玻璃棒的作用解答.
解答 解:
(1)混合物加水后试管壁发热,但是Ca(OH)2、CaCO3和Na2CO3加入水中不会放出热量,所以猜想二不成立.
(2)浑浊液中的滤渣中滴加盐酸,产生气泡,说明混合物中有碳酸钙,滤液中滴加盐酸有气泡,加澄清石灰水有沉淀生成,说明滤液中有碳酸钠,碳酸钠能与氢氧化钙反应生成碳酸钙沉淀和和氢氧化钠,但是如果只有氧化钙和氢氧化钠就不会生成碳酸钙沉淀和碳酸钠,故猜想一不成立.
(3)从(2)中的推导可知,混合物中既有CaO和NaOH,也有CaCO3和Na2CO3,是部分变质;
(4)通过实验可知,碱石灰在空气中极易变质,应该密封保存,过滤操作C中玻璃棒起到了引流的作用.
故答案为:
(1)不成立;
(2)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH,Na2CO3,不成立;
(3)部分变质;
(4)密封,引流.
点评 在解此类题时,先根据题中的现象推出确定的物质,对于不确定的物质要设计实验进行验证.

练习册系列答案
相关题目
11.蔬菜、水果中大多含有维生素C(化学式C6H8O6).下列关于维生素C的说法中错误的是( )
| A. | 维生素C是氧化物 | |
| B. | 由碳、氢、氧三种元素组成 | |
| C. | 1个分子由6个碳原子、8个氢原子和6个氧原子构成 | |
| D. | 青少年要多吃蔬菜、水果来补充维生素C |
9.下列物质中,属于纯净物的是( )
| A. | 冰水混合物 | B. | 食醋 | C. | 碳酸饮料 | D. | 硫酸铜溶液 |
16.金属及合金是重要的工业级建筑材料.
(1)如表是A、B、C三种金属的部分物理性质,
①三种金属中最不适宜作导线的是金属B的密度小(填字母),远程高压输电线不用金属A而选用金属B,主要原因是>.
②C的合金通常可以做菜刀、锤子等,其合金的硬度>5(填“>”“<”或“=”).
(2)为了验证铝、铜、银三种金属的活动性顺序,设计了下列四种方案,其中可行的是①④(填序号).
①将铝、银分别浸入到硫酸铜溶液中②将银分别浸入到硫酸铝、硫酸铜溶液中
③将铜、银分别浸入到硫酸铝溶液中④将铜分别浸入到硫酸铝、硝酸银溶液中
(3)炼铁厂常以焦炭、赤铁矿石(主要成分是Fe2O3)、空气等为主要原料炼铁,请写出用一氧化碳与氧化铁炼铁的化学方程式.
(1)如表是A、B、C三种金属的部分物理性质,
| 性质 金属 | 导电性(100为标准) | 密度(g/cm3) | 熔点(℃) | 硬度(10为标准) |
| A | 99 | 8.92 | 1083 | 3 |
| B | 61 | 2.70 | 660 | 2.9 |
| C | 17 | 7.86 | 1535 | 5 |
②C的合金通常可以做菜刀、锤子等,其合金的硬度>5(填“>”“<”或“=”).
(2)为了验证铝、铜、银三种金属的活动性顺序,设计了下列四种方案,其中可行的是①④(填序号).
①将铝、银分别浸入到硫酸铜溶液中②将银分别浸入到硫酸铝、硫酸铜溶液中
③将铜、银分别浸入到硫酸铝溶液中④将铜分别浸入到硫酸铝、硝酸银溶液中
(3)炼铁厂常以焦炭、赤铁矿石(主要成分是Fe2O3)、空气等为主要原料炼铁,请写出用一氧化碳与氧化铁炼铁的化学方程式.
6.在下表A、B、C三组选项中,有一组物质能够实现如图所示的转化.请回答下列问题.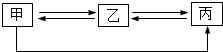
(1)选项中符合转化关系的是A(填序号).
(2)写出甲物质在生产或生活中的一种用途生成玻璃.

| 选项 | 甲 | 乙 | 丙 |
| A | Na2CO3 | CO2 | CaCO3 |
| B | NaOH | NaCl | NaNO3 |
| C | CuO | CuSO4 | Cu(OH)2 |
(2)写出甲物质在生产或生活中的一种用途生成玻璃.
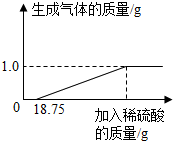 某兴趣小组对生锈废铁锅中铁的含量进行了测定.生锈的铁锅中除Fe、Fe2O3外,还含有碳、硅、锰等元素(提示:除Fe、Fe2O3以外的物质都不与稀硫酸反应).请按照要求完成实验过程.
某兴趣小组对生锈废铁锅中铁的含量进行了测定.生锈的铁锅中除Fe、Fe2O3外,还含有碳、硅、锰等元素(提示:除Fe、Fe2O3以外的物质都不与稀硫酸反应).请按照要求完成实验过程.
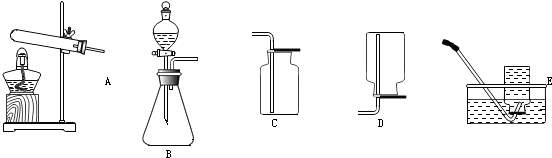
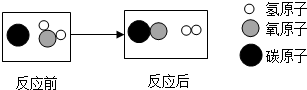 如图是高温下某反应的微观过程.
如图是高温下某反应的微观过程.