题目内容
8.某化学兴趣小组的同学在实验室以锌、稀硫酸和氧化铜为原料,先制取氢气,再用氢气还原氧化铜制取铜.关于该实验,有以下几种说法:①反应有红色物质生成
②实验不需要用到酒精灯
③用氢气还原氧化铜之前需要检验氢气的纯度
④利用该原料还可设计实验证明两种金属的活动性顺序
以上说法中,正确的个数有( )
| A. | 4个 | B. | 3个 | C. | 2个 | D. | 1个 |
分析 根据实验室中用锌和稀硫酸制取氢气并在加热的条件下还原氧化铜的现象以及注意事项来分析.
解答 解:锌和稀硫酸在常温下反应生成硫酸锌和氢气,在加热的条件下,氢气能将黑色的氧化铜还原为红色的铜.
①生成的铜是红色的,正确;
②氢气还原氧化铜需要用到酒精灯进行加热,错误;
③通入氢气前,一定要检验氢气的纯度,以防发生爆炸的危险,正确;
④氧化铜与稀硫酸反应生成硫酸铜和水,锌能置换成硫酸铜中的铜,说明锌比铜活泼,正确.
故选B.
点评 明确实验条件、实验现象以及实验的注意事项来分析,掌握化学基础知识是解题的关键.

练习册系列答案
 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
18.2015年2月28日,前央视记者柴静的《雾霾深度调查:穹顶之下》引发网友热议.形成雾霾天气的主要污染物是直径小于或等于2.5微米的悬浮颗粒物,即PM2.5.下列事实与形成PM2.5无关的是( )
| A. | 风力发电 | B. | 工业粉尘 | C. | 汽车尾气 | D. | 煤炭燃烧 |
3.下列变化属于化学变化的是( )
| A. | 冰融化成水 | B. | 胆矾研碎 | C. | 海水晒盐 | D. | 蜡烛燃烧 |
13.下列说法错误的是( )
| A. | 在复分解反应中生成物都是化合物 | B. | 分解反应一定有单质生成 | ||
| C. | 置换反应一定有新的单质生成 | D. | 中和反应一定有水生成 |
17.属于化学变化的是( )
| A. | 馒头发霉 | B. | 雪糕融化 | C. | 水果榨汁 | D. | 玻璃破碎 |
18.物质存放在对应的容器中,符合规范要求的是( )
| A. |  碳酸钙固体 | B. |  氯化钠溶液 | C. | 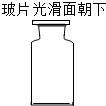 氧气 | D. | 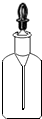 稀盐酸 |
 2014年6月10日是“全国低碳日”,“节能减排,低碳生活”的主题旨在倡导节约能源和利用清洁能源,减少温室气体二氧化碳的排放.下列做法符合“主题是C
2014年6月10日是“全国低碳日”,“节能减排,低碳生活”的主题旨在倡导节约能源和利用清洁能源,减少温室气体二氧化碳的排放.下列做法符合“主题是C