题目内容
11.如图为配置50g溶质质量分数为10%的氯化钠溶液的操作过程,下列有关操作与目的分析均正确的是( )
| 选项 | 操作 | 目的 |
| A | 用剩的食盐放回原试剂瓶 | 避免浪费 |
| B | 天平调平后在左、右托盘中各垫一张相同的纸 | 保证称取的食盐质量更准确 |
| C | 溶解时用玻璃棒搅拌 | 增加食盐的溶解能力 |
| D | 用50mL量筒替代天平量取所需的水 | 更加简便 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据实验室剩余药品的处理原则(三不一要),进行分析判断.
B、根据托盘天平的使用方法,进行分析判断.
C、根据溶解操作的方法,进行分析判断.
D、根据液体药品的取用方法,进行分析判断.
解答 解:A、对化学实验中的剩余药品,既不能放回原瓶,也不可随意丢弃,更不能带出实验室,应放入的指定的容器内;用剩的食盐放回原试剂瓶,以防止污染试剂,故选项说法错误.
B、天平调平后在左、右托盘中各垫一张相同的纸,是为了防止腐蚀托盘,故选项说法错误.
C、溶解时用玻璃棒搅拌,是为了加快溶解速率,而不是增加食盐的溶解能力,故选项说法错误.
D、用50mL量筒替代天平量取所需的水,更加简便、快速,故选项说法正确.
故选:D.
点评 本题难度不大,掌握配制溶质质量分数一定的溶液的实验步骤、各操作的注意事项等是正确解答本题的关键.

练习册系列答案
相关题目
1.空气成分中,约占总体积的21%是( )
| A. | N2 | B. | H2O | C. | O2 | D. | CO2 |
19. 根据氯化钠和硝酸钾的溶解度表,回答下列问题:
根据氯化钠和硝酸钾的溶解度表,回答下列问题:
(1)在20℃时,将50克氯化钠溶解到100克水中,形成的溶液的溶质质量分数为26.5%;
(2)当硝酸钾中混有少量氯化钠时,提纯硝酸钾所采用的方法是降温结晶;
(3)如图所示,小烧杯中盛放硝酸钾溶液,底部有少量未溶解的硝酸钾晶体,若将氢氧化钠固体投入到大烧杯的水中,不断搅拌,则小烧杯底部硝酸钾晶体的质量将减小(选填“增大”、“减小”或“不变”).
 根据氯化钠和硝酸钾的溶解度表,回答下列问题:
根据氯化钠和硝酸钾的溶解度表,回答下列问题:| 名称 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ |
| 氯化钠 | 35.8g | 36.0g | 36.3g | 36.6g | 37.0g | 37.3g | 37.8g |
| 硝酸钾 | 20.9g | 31.6g | 45.8g | 63.9g | 85.5g | 110g | 138g |
(2)当硝酸钾中混有少量氯化钠时,提纯硝酸钾所采用的方法是降温结晶;
(3)如图所示,小烧杯中盛放硝酸钾溶液,底部有少量未溶解的硝酸钾晶体,若将氢氧化钠固体投入到大烧杯的水中,不断搅拌,则小烧杯底部硝酸钾晶体的质量将减小(选填“增大”、“减小”或“不变”).
6.下列物质的化学式与分类都正确的一组是( )
| A. | 纯碱--Na2CO3--碱 | B. | 大理石--CaCO3--盐 | ||
| C. | 熟石灰--CaOH--碱 | D. | 硫酸--H2SO3--酸 |
3.下列实验过程中与图象描述相符的一组是( )
| A. | 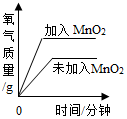 两份等质量、等溶质质量分数的双氧水溶液在有无MnO2的情况下产生 两份等质量、等溶质质量分数的双氧水溶液在有无MnO2的情况下产生 | |
| B. | 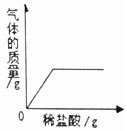 向部分变质的氢氧化钠溶液中滴加稀盐酸 向部分变质的氢氧化钠溶液中滴加稀盐酸 | |
| C. | 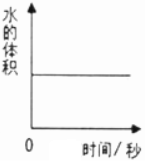 用燃磷法测定空气中氧气的含量 用燃磷法测定空气中氧气的含量 | |
| D. | 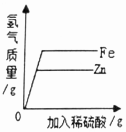 向等质量的铁、锌中分别加入稀硫酸 向等质量的铁、锌中分别加入稀硫酸 |
20.下列对物质的溶解性的描述中,错误的是( )
| A. | 物质的溶解性有强有弱,强弱不同 | |
| B. | 在一定条件下,一定量的水中,物质不能够无限的溶解 | |
| C. | 溶解性大小只与物质的性质有关,跟其他因素无关 | |
| D. | 物质的溶解性是指一种物质在另一种物质中的溶解能力 |
 物质的量是一种物理量,其单位是摩尔(mol),1摩尔物质大约含有6.02×1023个该物质的微粒.如1mol氢气含有6.02×1023个H2分子,含有2×6.02×1023个H原子.据此回答:
物质的量是一种物理量,其单位是摩尔(mol),1摩尔物质大约含有6.02×1023个该物质的微粒.如1mol氢气含有6.02×1023个H2分子,含有2×6.02×1023个H原子.据此回答: