题目内容
12. Q盐溶液能给酸X、碱Y、盐Z进行如图所示的反应.请推断并写出符合要求的三个化学反应的方程式.
Q盐溶液能给酸X、碱Y、盐Z进行如图所示的反应.请推断并写出符合要求的三个化学反应的方程式.(1)Na2CO3+2HCl═NaCl+H2O+CO2↑;
(2)Na2CO3+Ca(OH)2═2NaOH+CaCO3↓;
(3)Na2CO3+CaCl2═2NaCl+CaCO3↓.
分析 根据Q盐溶液能与酸溶液X反应生成无色气体,所以Q中含有碳酸根离子,Q会碱溶液反应生成白色沉淀后,所以碱中含有钙离子或钡离子,所以Q盐溶液可能是碳酸钠,碱溶液Y可能是氢氧化钙,碳酸钠和氯化钙反应会生成碳酸钙沉淀,所以Z可能是氯化钙,然后将推出的物质进行验证即可.
解答 解:Q盐溶液能与酸溶液X反应生成无色气体,所以Q中含有碳酸根离子,Q会碱溶液反应生成白色沉淀后,所以碱中含有钙离子或钡离子,所以Q盐溶液可能是碳酸钠,碱溶液Y可能是氢氧化钙,碳酸钠和氯化钙反应会生成碳酸钙沉淀,所以Z可能是氯化钙,经过验证,推导正确,所以
(1)碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:Na2CO3+2HCl═NaCl+H2O+CO2↑;
(2)碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Na2CO3+Ca(OH)2═2NaOH+CaCO3↓;
(3)碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,化学方程式为:Na2CO3+CaCl2═2NaCl+CaCO3↓.
故答案为:(1)Na2CO3+2HCl═NaCl+H2O+CO2↑;
(2)Na2CO3+Ca(OH)2═2NaOH+CaCO3↓;
(3)Na2CO3+CaCl2═2NaCl+CaCO3↓.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.关注健康,预防疾病.下列叙述正确的是( )
| A. | 氧、碳、氢、铁、氮、镁、钙都是人体中含有的常量元素 | |
| B. | 缺乏维生素A会引起坏血病 | |
| C. | 如果人体摄入的糖类过多,不仅容易发胖,还可能诱发疾病 | |
| D. | 老年人缺钙会患佝偻病 |
20.下列化学符号中,数字“2”表示的意义不正确的是( )
| A. | 2O:2个氧分子 | B. | H2O:1个水分子中有2个氢原子 | ||
| C. | $\stackrel{+2}{Ca}$:正二价的钙元素 | D. | Mg2+:1个镁离子带2个单位正电荷 |
7.实验室欲制取少量Fe2(SO4)3溶液,下列四项中哪项为最佳选择( )
| A. | 过量Fe粉与稀H2SO4 反应 | B. | 过量Fe2O3与稀H2SO4反应 | ||
| C. | 过量稀H2SO4 与Fe粉反应 | D. | 过量稀H2SO4与Fe2O3反应 |
17.除去下列各物质中的少量杂质所选用的试剂均正确的是( )
| 项目 | 物质 | 杂质 | 试剂 | 操作方法 |
| A | 木炭粉 | MnO2 | 足量的水 | 溶解、过滤、蒸发 |
| B | O2 | 水蒸气 | 适量NaOH溶液 | 洗气 |
| C | NaOH | Na2CO3 | 适量的稀盐酸 | 不再产生气体时停止 |
| D | 稀盐酸 | H2SO4 | 适量的BaCl2溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
2.下列有关资源与环境的说法,错误的是( )
| A. | 用洗脸水冲厕所,将废报纸、废旧金属等送到废品回收站 | |
| B. | 水在自然界中不断循环,淡水资源取之不尽,用之不竭 | |
| C. | 未来的理想能源必须足够安全,清洁,可以保证不会严重影响环境 | |
| D. | 回收塑料制品既能节约石油资源,又能减少白色污染 | |
| E. | 回收塑料制品既能节约石油资源,又能减少白色污染 |

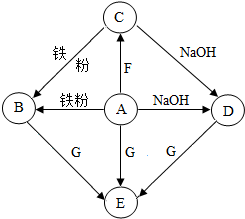 A-G是初中化学常见物质.其中,A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀.如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.
A-G是初中化学常见物质.其中,A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀.如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.