题目内容
13.常用实验室制取氧气的方法有:a.加热氯酸钾和二氧化锰粉末;b.加热高锰酸钾固体;c.用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生氧气.
(1)写出图A中指定仪器的名称:①试管;②酒精灯;
(2)请仔细分析上图中装置A的特点,推测该装置可用于上述制氧气方法的有b (填a、b或c);
(3)采用方法c制取氧气应该选用的气体发生装置是上图中的B(填“A”或“B”);
(4)利用装置A制氧气,在结束实验时要先撤离导管出水面,再熄灭酒精灯,其目的是防止水倒流进试管引起试管炸裂;利用装置B制氧气时,长颈漏斗的下端要插入液面以下,其目的是防止产生的气体从长颈漏斗逸出.
分析 据图即可知道有关仪器的名称;根据氧气的实验室制取以及实验装置的选择方法进行分析解答即可.
解答 解:(1)据图可以看出,①是试管,②是酒精灯,故填:试管,酒精灯;
(2)A装置是固体加热反应,试管口有一团棉花,故是加热高锰酸钾制取氧气,故填:b;
(3)用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生氧气,是固液常温型反应,故选则B装置制取,故填:B;
(4)用装置A制氧气,在结束实验时要先撤离导管出水面,再熄灭酒精灯,是为了防止水倒流进试管引起试管炸裂,用装置B制氧气时,长颈漏斗的下端要插入液面以下是为了防止产生的气体从长颈漏斗逸出,故填:防止水倒流进试管引起试管炸裂;防止产生的气体从长颈漏斗逸出.
点评 本题考查的是常见气体的实验室制取的知识,完成此题,可以依据已有的气体制取的知识进行.

练习册系列答案
相关题目
8.研究和控制化学反应条件有重要意义.
(1)同学们想探究双氧水的浓度对反应速率的影响.在其他条件相同的情况下进行了三次实验.记录各收集一瓶相同体积氧气所需要的时间.
①取用二氧化锰的仪器是图1中的B

②写出上述反应的文字表达式过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
③实验3中,加入二氧化锰的质量为5g.
④相同条件下,实验3产生氧气的速率最快,说明其他条件相同时,反应物的浓度越高,反应速率越快.
(2)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择如图2装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中水蒸气含量太高.
(1)同学们想探究双氧水的浓度对反应速率的影响.在其他条件相同的情况下进行了三次实验.记录各收集一瓶相同体积氧气所需要的时间.
| 实验 | 30%双氧水的质量(g) | 加入水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 67 |

②写出上述反应的文字表达式过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
③实验3中,加入二氧化锰的质量为5g.
④相同条件下,实验3产生氧气的速率最快,说明其他条件相同时,反应物的浓度越高,反应速率越快.
(2)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择如图2装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中水蒸气含量太高.
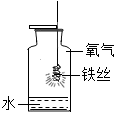 分析如图所示的实验,回答:铁丝在氧气中燃烧,观察到的现象是剧烈燃烧、火星四射、放出热量、生成黑色固体,铁丝绕成螺旋状的目的是增大与氧气的接触面积,使铁燃烧更充分,集气瓶瓶底放入少许水的目的是防止溅落的熔化物炸裂瓶底.若将氧气换成空气,则该反应不能进行(填“能”或“不能”),原因是某些在空气中不能燃烧的物质,在氧气中却能燃烧.写出反应的表达式:铁+氧气$\stackrel{点燃}{→}$四氧化三铁.
分析如图所示的实验,回答:铁丝在氧气中燃烧,观察到的现象是剧烈燃烧、火星四射、放出热量、生成黑色固体,铁丝绕成螺旋状的目的是增大与氧气的接触面积,使铁燃烧更充分,集气瓶瓶底放入少许水的目的是防止溅落的熔化物炸裂瓶底.若将氧气换成空气,则该反应不能进行(填“能”或“不能”),原因是某些在空气中不能燃烧的物质,在氧气中却能燃烧.写出反应的表达式:铁+氧气$\stackrel{点燃}{→}$四氧化三铁.
 某化学兴趣小组用如图所示装置测定空气中氧气的体积分数,请回答下列问题:
某化学兴趣小组用如图所示装置测定空气中氧气的体积分数,请回答下列问题:
 实验室利用如图所示装置进行加热氯酸钾制氧气的实验.
实验室利用如图所示装置进行加热氯酸钾制氧气的实验.