题目内容
6.有A、B、C、D四种元素.当A元素的原子失去3个电子、B元素的原子得到2个电子都形成电子排布跟氖原子相同的粒子.C元素原子在第三层上的电子数比第二层上的电子数少一个.D元素原子内无中子.(1)写出这四种元素的符号:A是Al,B是O,C是Cl,D是H.
(2)D单质在B单质中燃烧,发出淡蓝色的火焰.
(3)写出A和C元素组成化合物的化学式是AlCl3.
分析 根据题意,当A元素的原子失去3个电子、B元素的原子得到2个电子都形成电子排布跟氖原子相同的粒子,氖原子的核外有10个电子,则A元素的原子核外电子数应为10+3=13,B元素原子的核外电子数应为10-3=8;C元素原子在第三层上的电子数比第二层上的电子数少一个,第二层的电子数为8,则第三层上的电子数为8-1=7;D元素原子内无中子,则D原子为氢原子;据此进行分析解答.
解答 解:当A元素的原子失去3个电子、B元素的原子得到2个电子都形成电子排布跟氖原子相同的粒子,氖原子的核外有10个电子,则A元素的原子核外电子数应为10+3=13,B元素原子的核外电子数应为10-3=8;则A、B元素的原子的核内质子数为13、8,分别为铝元素、氧元素.C元素原子在第三层上的电子数比第二层上的电子数少一个,第二层的电子数为8,则第三层上的电子数为8-1=7;则其原子核外电子数为17,其核内质子数为17,其氯元素.D元素原子内无中子,则D原子为氢原子.
(1)这四种元素的符号分别是Al、O、Cl、H.
(2)D单质在B单质中燃烧,即氢气在氧气中燃烧,产生淡蓝色火焰.
(3)A和C元素组成化合物,即铝元素和氯元素,能形成氯化铝,铝元素显+3价,氯元素显-1价,其化学式为:AlCl3.
故答案为:(1)Al、O、Cl、H;(2)淡蓝;(3)AlCl3.
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.

练习册系列答案
相关题目
16.下列物质直接由原子构成的是( )
| A. | 二氧化碳(CO2) | B. | 汞 (Hg) | C. | 氧气( O2 ) | D. | 水(H2O) |
17.下列关于原子、分子的叙述,正确的是( )
①分子、原子都是构成物质的粒子
②分子大、原子小
③分子之间有间隔,原子之间没有间隔
④分子能保持物质的化学性质,原子不能
⑤分子在化学变化中可以再分,原子在化学变化中不可以再分
⑥分子、原子都在不停地运动.
①分子、原子都是构成物质的粒子
②分子大、原子小
③分子之间有间隔,原子之间没有间隔
④分子能保持物质的化学性质,原子不能
⑤分子在化学变化中可以再分,原子在化学变化中不可以再分
⑥分子、原子都在不停地运动.
| A. | ①②③ | B. | ②③④ | C. | ④⑤⑥ | D. | ①⑤⑥ |
18.从分子的角度分析并解释下列事实,不正确的是( )
| 选项 | 事实 | 解释 |
| A | 氧化汞分解成汞和氧气 | 在化学变化中分子可以再分 |
| B | 端午时节粽飘香 | 分子在不断运动着 |
| C | 气体受热膨胀 | 温度升高,分子自身体积增大 |
| D | 干冰升华 | 碘分子间的间隔变大 |
| A. | A | B. | B | C. | C | D. | D |
16.下列各组离子在溶液中能大量共存的是( )
| A. | Ca2+ Cl- Na+ CO32- | B. | NH4+ K+ NO3- OH- | ||
| C. | H+ Na+ SO42- CO32- | D. | K+ Na+ NO3- SO42- |
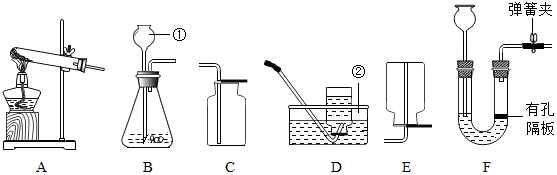
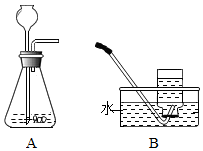 结合如图实验装置图回答问题:
结合如图实验装置图回答问题: 硫酸是工农业生产中使用非常广泛的一种试剂,实验室用质量分数为98%的浓硫酸(密度为1.84g/cm3)配制49g质量分数为20%的硫酸.
硫酸是工农业生产中使用非常广泛的一种试剂,实验室用质量分数为98%的浓硫酸(密度为1.84g/cm3)配制49g质量分数为20%的硫酸.