题目内容
18.课外活动小组的同学在测定由NaCl和Na2CO3形成的固体混合物组成时,进行了以下实验:取40g固体混合物配成溶液,平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见表:| 实验一 | 实验二 | 实验三 | 实验四 | |
| 原固体混合物质量 | 10g | 10g | 10g | 10g |
| 加入CaCl2溶液质量 | 10g | 20g | 30g | 40g |
| 生成的沉淀的质量 | 2g | m | 5g | 5g |
(1)m=4g;
(2)原固体混合物中Na2CO3的质量是多少?所加CaCl2溶液的质量分数是多少?
分析 (1)根据实验数据,加入10gCaCl2溶液完全反应可生成沉淀质量为2g,加入30gCaCl2溶液时仍有沉淀生成,可判断表中m的值;
(2)加入氯化钙溶液至完全反应时,生成沉淀质量为5g,根据碳酸钠与氯化钙反应的化学方程式,可由生成沉淀碳酸钙的质量计算中原固体混合物中Na2CO3的质量,根据反应的化学方程式,可以得到各物质之间的比例关系,利用沉淀的质量进而求出氯化钙的质量,从而求出CaCl2溶液的溶质质量分数.
解答 解:
(1)分析实验数据可知,每加入10g氯化钙溶液可生成2g沉淀,因此加入20g氯化钙溶液时,得到沉淀质量m=2g×$\frac{20g}{10g}$=4g
(2)设10g原固体混合物中Na2CO3质量为x
CaCl2+Na2CO3═CaCO3↓+2NaCl
106 100
x 5g
$\frac{106}{x}$=$\frac{100}{5g}$
x=5.3g
由表中数据可知:10gCaCl2溶液最多生成沉淀质量为2g,设CaCl2的质量为x
CaCl2+Na2CO3=CaCO3↓+2NaCl
111 100
x 2g
$\frac{111}{x}$=$\frac{100}{2g}$
x=2.22g
CaCl2溶液的溶质质量分数=$\frac{2.22g}{10g}$×100%=22.2%
故答案为:(1)4g
(2)5.3g;22.2%
点评 本题主要考查学生对化学方程式的书写,能够根据化学方程式判断现象及生成的物质,熟悉完全反应及不完全反应的概念,并能据此查找数据,进行计算.

练习册系列答案
相关题目
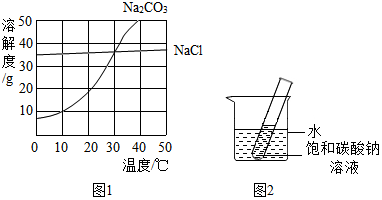
3. 图为硫酸钠和氯化铵的溶解度曲线.下列说法正确的是( )
图为硫酸钠和氯化铵的溶解度曲线.下列说法正确的是( )
 图为硫酸钠和氯化铵的溶解度曲线.下列说法正确的是( )
图为硫酸钠和氯化铵的溶解度曲线.下列说法正确的是( )| A. | 40℃时硫酸钠的溶解度是50 | |
| B. | 40℃时硫酸钠饱和溶液的质量分数最大 | |
| C. | 硫酸钠的溶解度随着温度升高而不断增大 | |
| D. | 降低温度一定能使硫酸钠不饱和溶液变成饱和溶液 |
10.牙膏是由多种无机物和有机物组成的,它包括摩擦剂、洗涤泡沫剂、粘合剂、保湿剂、甜味剂、芳香剂和水分.其中摩擦剂是牙膏的主体,常用的摩擦剂有碳酸钙、氢氧化铝、二氧化硅,用量在30%-50%之间.
某探究小组对牙膏进行了如下探究:
(1)摩擦剂成分的探究:
①提出猜想:如果牙膏中摩擦剂只含有一种成分,则:
假设1:摩擦剂可能是氢氧化铝;
假设2:摩擦剂可能是碳酸钙;
假设3:摩擦剂可能是二氧化硅.
②[实验验证]取少量某牙膏于烧杯中,并加入过量的稀盐酸,则实验中出现的现象与对应结论如下表:(注:二氧化硅既不溶于水又不溶于酸.)
(2)牙膏中碳酸钙质量分数的探究
实验用品:牙膏(含碳酸钙)、稀盐酸、天平、烧杯、试管、玻璃棒.
实验步骤:
取某牙膏100.0g放入烧杯中,再加入400.0g稀盐酸(足量),充分方应后所得混合物的质量为478.0g.试求:①反应产生的二氧化碳多少克?②碳酸钙在此牙膏中的质量分数是多少?(化学反应方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑)
某探究小组对牙膏进行了如下探究:
| ③实验中出现的现象 | 结 论 |
| 产生大量气泡 | 假设2成立 |
①提出猜想:如果牙膏中摩擦剂只含有一种成分,则:
假设1:摩擦剂可能是氢氧化铝;
假设2:摩擦剂可能是碳酸钙;
假设3:摩擦剂可能是二氧化硅.
②[实验验证]取少量某牙膏于烧杯中,并加入过量的稀盐酸,则实验中出现的现象与对应结论如下表:(注:二氧化硅既不溶于水又不溶于酸.)
(2)牙膏中碳酸钙质量分数的探究
实验用品:牙膏(含碳酸钙)、稀盐酸、天平、烧杯、试管、玻璃棒.
实验步骤:
取某牙膏100.0g放入烧杯中,再加入400.0g稀盐酸(足量),充分方应后所得混合物的质量为478.0g.试求:①反应产生的二氧化碳多少克?②碳酸钙在此牙膏中的质量分数是多少?(化学反应方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑)
8.区别下列各组物质,所用的试剂或方法错误的是( )
| A. | 金与铜锌合金--稀盐酸 | B. | 硬水与软水--肥皂水 | ||
| C. | 水与澄清石灰水--二氧化碳气体 | D. | 氮气与二氧化碳--燃着的木条 |
 为了探究碱的性质,甲乙两组同学向相同体积的石灰水和烧碱溶液中分别通入C02气体.观察到前者变浑浊.后者无明显现象.甲组同学认为C02能与石灰水反应,但不能与烧碱溶液反应.而乙组同学认为C02也能与烧碱溶液发生反应.
为了探究碱的性质,甲乙两组同学向相同体积的石灰水和烧碱溶液中分别通入C02气体.观察到前者变浑浊.后者无明显现象.甲组同学认为C02能与石灰水反应,但不能与烧碱溶液反应.而乙组同学认为C02也能与烧碱溶液发生反应.
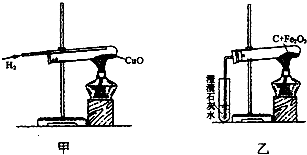 如图甲是氢气和氧化铜反应的实验,图乙是木炭和氧化铁反应的实验.
如图甲是氢气和氧化铜反应的实验,图乙是木炭和氧化铁反应的实验.