题目内容
氢气和氧气的混合气体共20g,在点燃的条件下,让它们充分反应后,生成9g水,则原混合气体中含有氢气的质量可能是
- A.8g
- B.12g
- C.11g
- D.无法确定
B
分析:氧气参加的反应两种情况:过量和全反应,写出化学方程式并代入数据计算即可.
解答:设生成水9g,消耗氧气的质量是x,消耗氢气的质量是y,
2H2+O2 2H2O
2H2O
4 32 36
y x 9g
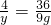
y=1g

x=8g
所以氢气的质量是20g-8g=12g(此时氧气相对于氢气不足),或者氢气的质量是1g(此时氧气相对于氢气过量).
故选B.
点评:注意氧气是否全部参加反应,因此要先计算恰好反应时氧气和氢气的质量,然后计算氢气的质量.
分析:氧气参加的反应两种情况:过量和全反应,写出化学方程式并代入数据计算即可.
解答:设生成水9g,消耗氧气的质量是x,消耗氢气的质量是y,
2H2+O2
 2H2O
2H2O4 32 36
y x 9g
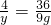
y=1g

x=8g
所以氢气的质量是20g-8g=12g(此时氧气相对于氢气不足),或者氢气的质量是1g(此时氧气相对于氢气过量).
故选B.
点评:注意氧气是否全部参加反应,因此要先计算恰好反应时氧气和氢气的质量,然后计算氢气的质量.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
将氢气和氧气的混合气体共10g点燃,充分反应后生成9g水.则原混合气体中氢气和氧气的质量分别是( )
| A、2g、8g | B、2.5g、7.5g | C、5g、5g | D、1g、9g |
