题目内容
 如图是一则化肥广告:硫酸铵中氮元素:氢元素:硫元素:氧元素的质量比是
如图是一则化肥广告:硫酸铵中氮元素:氢元素:硫元素:氧元素的质量比是考点:元素质量比的计算,元素的质量分数计算
专题:化学式的计算
分析:根据广告图可知物质的化学式,利用相对原子质量来计算元素的质量比;计算氮元素的质量分数,根据氮元素的质量分数来判断广告的真实性;
解答:解:硫酸铵中氮元素:氢元素:硫元素:氧元素质量比为(14×2):(1×4×2):32:(16×4)=7:2:8:16;
(NH4)2SO4中氮元素的质量分数为=
×100%=21.2%<34.1%,
即纯硝酸铵中氮元素的质量分数小于34.1%,则该广告是虚假广告;
答案:7:2:8:16;21.2%,虚假;
(NH4)2SO4中氮元素的质量分数为=
| 14×2 |
| 14×2+1×4×2+32+16×4 |
即纯硝酸铵中氮元素的质量分数小于34.1%,则该广告是虚假广告;
答案:7:2:8:16;21.2%,虚假;
点评:本题利用化肥广告来考查学生利用信息中物质的化学式进行计算,抓住化学式是解答的关键,熟悉常见原子的相对原子质量来计算即可.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
固城湖是我们的“母亲湖”,固城湖水养育了一代又一代勤劳的高淳人民,为我县创造出了很多的财富.下列关于水的说法中不正确的是( )
| A、用活性炭吸附水中的异味和色素 |
| B、城市污水必须经过净化处理后才能排放 |
| C、水资源是宝贵的,一定要节约用水 |
| D、清澈、透明的固城湖水是纯净物 |
金刚石、石墨都是由碳元素组成的物质,化学性质相同,而物理性质不同的原因是( )
| A、同种元素组成,但原子排列不同 |
| B、原子结构相同 |
| C、相对原子质量相同 |
| D、原子最外层电子数相同 |
下列防止空气污染、防止水污染的措施不正确的是( )
| A、大力植树造林 |
| B、提倡使用太阳能、风能等清洁能源 |
| C、禁止使用化肥和农药 |
| D、禁止使用含磷的洗涤剂 |
如图所示是实验室常用的仪器,请用图中仪器的名称按要求填空:
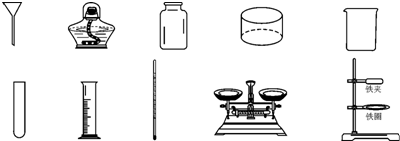
(1)用 量取50mL水,倒入 中,且用 加热水时需垫上石棉网.
(2)收集少量气体用 ;快速加热 内盛有的少量液体;用 称量10.5g的固体.

(1)用
(2)收集少量气体用
下列物质的性质与对应的用途没有关系的是( )
| A、氧气助燃------作燃料 |
| B、氮气的化学性质稳定----------作保护气 |
| C、铜能导电-------可作电线 |
| D、二氧化碳能与水反应--------人工降雨 |