题目内容
11.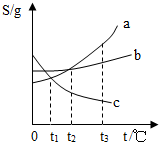 现有溶解度曲线如图,下列有关说法正确的是( )
现有溶解度曲线如图,下列有关说法正确的是( )| A. | t2℃时a、b两物质溶液的溶质质量分数相等 | |
| B. | 将c的不饱和溶液降温可以转化为饱和溶液 | |
| C. | 将t3℃时a、b、c三种物质的饱和溶液降温到t1℃时,所得溶液的溶质质量分数大小顺序为b>a>c | |
| D. | 将t3℃的a、b、c 三种物质的饱和溶液冷却到t1 时,a物质析出最多,无c物质析出 |
分析 A、不知溶液中溶质、溶剂的质量多少,无法判断溶液中溶质质量分数大小;
B、根据c物质的溶解度随温度的降低而增大进行解答;
C、根据三种物质的溶解度随温度变化情况及饱和溶液中溶质的质量分数计算方法进行解答;
D、不知道a、b、c物质的饱和溶液的质量大小,所以不能判断出析出晶体的多少进行解答.
解答 解:A、不知溶液中溶质、溶剂的质量多少,无法判断溶液中溶质质量分数大小,故错误;
B、c物质的溶解度随温度的降低而增大,所以将c的不饱和溶液升温可以转化为饱和溶液,故错误;
C、将t3℃时a、b、c三种物质的饱和溶液降温到t1℃时,ab的溶解度减小析出晶体,溶液中溶质质量减小,溶剂质量不变,溶质质量分数减小,c的溶解度变大,溶液中溶质、溶剂质量不变,溶质的质量分数与降温前相等;饱和溶液中溶质的质量分数的计算式$\frac{溶解度}{溶解度+100g}$×100%,可知溶解度大则溶质的质量分数大,而t1℃时b的溶解度大于a的溶解度大于降温前c的溶解度,故所得溶液的溶质质量分数大小顺序为b>a>c,正确;
D、不知道三种物质的饱和溶液的质量大小,所以不能判断出析出晶体的多少,故错误;
故选:C.
点评 利用溶解度曲线图可以判断在不同的温度下同一固体物质溶解度受温度的影响情况,也可以判断不同物质在同一温度下的大小情况等知识,能较好考查学生分析、解决问题的能力.

练习册系列答案
相关题目
1.在化学反应前后有元素化合价发生变化的反应属于氧化还原反应.例如:在$\stackrel{+2}{Cu}$O+$\stackrel{0}{H}$2 $\frac{\underline{\;\;△\;\;}}{\;}$$\stackrel{0}{Cu}$+$\stackrel{+1}{H}$2O中,反应前后Cu和H的化合价发生了变化,该反应是氧化还原反应.根据以上信息判断下列化学反应中不属于氧化还原反应的是( )
| A. | CaCO3$\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑ | B. | 2H2+O2 $\frac{\underline{\;点燃\;}}{\;}$2H2O | ||
| C. | Fe+CuSO4═Cu+FeSO4 | D. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2 |
19.下列说法正确的是( )
| A. | K2MnO4、KMnO4、MnO2三者中Mn元素的化合价逐渐升高 | |
| B. | HCl、NaCl、Na2CO3溶液的pH逐渐变大 | |
| C. | NH4NO3、NaCl、CaO三者溶于水后,所得溶液的温度逐渐降低 | |
| D. | 将Zn、Fe两金属片分别放入CuSO4溶液中可以证明三种金属的活动性顺序为Zn>Fe>Cu |
16.下列实验方法正确的是( )
| A. | 用稀盐酸除去热水瓶胆中的水垢(主要成分是碳酸钙和氢氧化镁) | |
| B. | 用过量的锌粉除去氯化铜溶液中混有的少量氯化锌 | |
| C. | 用pH试纸测定二氧化碳的酸碱度 | |
| D. | 用酚酞溶液鉴别食盐水和稀盐酸 |
 如图是a、b、c三种物质溶解度曲线,a与c溶解度曲线相交于P点.据图回答:
如图是a、b、c三种物质溶解度曲线,a与c溶解度曲线相交于P点.据图回答:
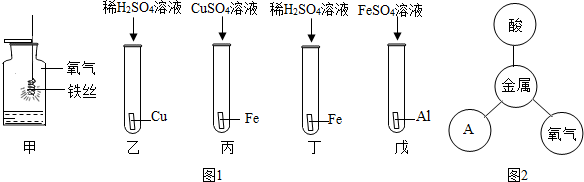

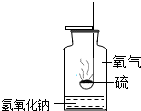 根据硫在氧气中燃烧的示意图用化学用语填空:
根据硫在氧气中燃烧的示意图用化学用语填空: