题目内容
20.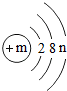 某粒子(原子或离子)的结构示意图为,请回答下列问题:
某粒子(原子或离子)的结构示意图为,请回答下列问题:(1)若n=3,则m=13;该元素氧化物的化学式为Al2O3
(2)若该粒子为电中性,则n的最大值为8;
(3)若m=12则该粒子对应的元素在化合物中的化合价为+2;
(4)若m=17,且该粒子为食盐的主要成分中的一种组成微粒,则该粒子的化学符号为Cl-.
分析 (1)n=3,结合当质子数=核外电子数,为原子,进行分析解答.
(2)若该粒子为电中性,即该粒子为原子,最外层电子数最多为8,进行分析解答.
(3)若m=12,则n=12-2-8=2,结合化合价的数值等于离子所带电荷的数值,且符号一致,进行分析解答.
(4)若m=17,为氯元素,食盐的主要成分氯化钠是由钠离子和氯离子构成的,据此进行分析解答.
解答 解:(1)n=3,则m=2+8+3=13,为铝元素;该元素氧化物中,铝元素显+3价,氧元素显-2价,其化学式为:Al2O3.
(2)若该粒子为电中性,即该粒子为原子,最外层电子数最多为8,则n的最大值为8.
(3)若m=12,则n=12-2-8=2,原子的最外层电子数为2,在化学反应中易失去2个电子而形成带2个单位正电荷的阳离子,化合价的数值等于离子所带电荷的数值,且符号一致,则则该元素的化合价为+2价.
(4)食盐的主要成分氯化钠是由钠离子和氯离子构成的,m=17,且该粒子为食盐的主要成分中的一种组成微粒,则该粒子为氯离子,其离子符号为:Cl-.
故答案为:(1)13;Al2O3;(2)8;(3)+2;(4)Cl-.
点评 本题难度不大,考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键.

练习册系列答案
相关题目
10.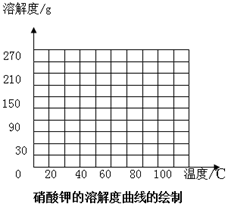 硝酸钾在不同温度时的溶解度如下:
硝酸钾在不同温度时的溶解度如下:
你能将硝酸钾的溶解度随温度变化的关系在图上表示出来吗?
 硝酸钾在不同温度时的溶解度如下:
硝酸钾在不同温度时的溶解度如下:| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
5. “双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图14所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,展开了实验探究.请你一起参与探究活动,并填写题中空白.
“双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图14所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,展开了实验探究.请你一起参与探究活动,并填写题中空白.
【提出问题】久置“双吸剂”的成分是什么?
【做出猜想】久置“双吸剂”中可能有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
【实验探究1】取固体样品研磨,用磁铁吸引,磁铁上沾有黑色粉末,说明“双吸剂”中一定有Fe.再用磁铁反复吸引后,残留固体用于后续探究活动.
【实验探究2】
【反思提高】
(1)请写出【探究2】操作3中所涉及的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑,3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)有同学提出【探究2】操作2中得出的结论不合理,理由是CaO+H2O=Ca(OH)2.(用方程式表示)
 “双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图14所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,展开了实验探究.请你一起参与探究活动,并填写题中空白.
“双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图14所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,展开了实验探究.请你一起参与探究活动,并填写题中空白.【提出问题】久置“双吸剂”的成分是什么?
【做出猜想】久置“双吸剂”中可能有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
【实验探究1】取固体样品研磨,用磁铁吸引,磁铁上沾有黑色粉末,说明“双吸剂”中一定有Fe.再用磁铁反复吸引后,残留固体用于后续探究活动.
【实验探究2】
| 实验操作 | 实验现象 | 实验结论 |
| 1.将实验探究1中残留固体中加入足量水充分溶解 | 固体部分溶解,并放出热量 | 固体中一定含有CaO; |
| 2.过滤,向滤液中滴加几滴无色酚酞试液 | 无色变红色 | 固体中一定含有Ca(OH)2 |
| 3.取过滤后滤渣,加入足量稀盐酸 | 1.产生大量气泡 2.溶液由无色变为黄色 | 固体中一定有CaCO3和 Fe2O3. |
(1)请写出【探究2】操作3中所涉及的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑,3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)有同学提出【探究2】操作2中得出的结论不合理,理由是CaO+H2O=Ca(OH)2.(用方程式表示)
9.区分生活中的下列各组物质,所用方法完全正确的是( )
| 需区分物质 | 方法一 | 方法二 | |
| A | 硝酸铵和碳酸氢铵 | 直接闻气味 | 加盐酸观察现象 |
| B | 氯化氢和氨气 | 直接闻气味 | 通入水中观察溶解性 |
| C | 羊毛和涤纶 | 点燃闻气味 | 观察色泽硬度弹性 |
| D | 铝丝和银丝 | 加入盐酸中观察 | 伸入硫酸铜固体中观察 |
| A. | A | B. | B | C. | C | D. | D |
19.下列各组概念中,前者包括后者的是( )
| A. | 氧化物、单质 | B. | 纯净物、化合物 | C. | 化合物、混合物 | D. | 氧化物、化合物 |