题目内容
1.以盐酸为例,列表梳理酸的4条化学性质,写出相关的化学方程式.(指示剂与酸和碱反应的不写)①Fe+2HCl═FeCl2+H2↑ ②Fe2O3+6HCl═2FeCl3+3H2O
③3HCl+Al(OH)3═AlCl3+3H2O ④Na2CO3+2HCl═2NaCl+H2O+CO2↑.
分析 根据酸会与活泼金属反应生成盐和氢气,会与碱反应生成盐和水,会与金属氧化物反应生成盐和水,会与盐反应生成两种新盐进行分析.
解答 解:①:盐酸与金属反应:盐酸与铁反应生成氯化亚铁和氢气,化学方程式为:Fe+2HCl═FeCl2+H2↑;
②:盐酸与金属氧化物反应:盐酸与与氧化铁反应生成氯化铁和水,化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O;
③:盐酸与碱反应:盐酸与与氢氧化铝反应生成氯化铝和水,化学方程式为:3HCl+Al(OH)3═AlCl3+3H2O;
④:盐酸与盐反应:盐酸与碳酸钠反应生成氯化钠、水和二氧化碳,化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
故答案为:①Fe+2HCl═FeCl2+H2↑;
②Fe2O3+6HCl═2FeCl3+3H2O;
③3HCl+Al(OH)3═AlCl3+3H2O;
④Na2CO3+2HCl═2NaCl+H2O+CO2↑.
点评 归纳是把零碎的化学知识和一些物质的性质系统到一起,这样对学习好化学知识又很大帮助.

练习册系列答案
相关题目
16.分析推理是化学学习中常用的思维方法.下列说法正确的是( )
| A. | 碱性溶液能使酚酞试液变红,滴入酚酞试液后变红的溶液一定呈碱性 | |
| B. | 燃烧都伴随着发光、放热,所以有发光、放热现象的就是燃烧 | |
| C. | 盐是由金属离子和酸根离子组成的,硝酸铵中没有金属阳离子,不属于盐 | |
| D. | 分子、原子都是不显电性的粒子,但不显电性的粒子不一定是分子或原子 |
11.根据您的生活常识,请判断下列混合体系属于溶液的是( )
| A. | 菜汤 | B. | 石灰浆 | C. | 啤酒 | D. | 黄河水 |
 液化石油气是常用的燃料.请回答:
液化石油气是常用的燃料.请回答: 如图是简易电解水装置图,试回答问题:
如图是简易电解水装置图,试回答问题:
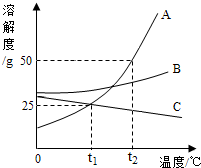 如图是A、B、C三种物质的溶解度曲线.
如图是A、B、C三种物质的溶解度曲线.