题目内容
10.下列物质分类的正确组合是( )| 碱 | 酸 | 盐 | 酸性氧化物 | |
| A | 纯碱 | 盐酸 | 烧碱 | 二氧化硫 |
| B | 烧碱 | 硫酸 | 食盐 | 一氧化碳 |
| C | 苛性钠 | 醋酸 | 石灰石 | 水 |
| D | 苛性钾 | 硝酸 | 苏打 | 三氧化硫 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据酸是指在电离时产生的阳离子全部是氢离子的化合物;单质是由一种元素组成的纯净物;碱是指在电离时产生的阴离子全部是氢氧根离子的化合物;氧化物是指有两种元素组成且一种是氧元素的化合物;据此进行分析判断.
解答 解:A、纯碱是碳酸钠,属于盐;烧碱是氢氧化钠,属于碱,故选项错误.
B、一氧化碳不属于酸性氧化物,故选项错误.
C、水不是酸性氧化物,故选项错误.
D、苛性钾属于碱;硝酸属于酸;苏打是碳酸钠,属于盐;三氧化硫属于酸性氧化物,故选项正确.
故选D.
点评 本题难度不大,考查物质类别的判别,抓住氧化物、酸、碱、单质的特征、熟悉常见的物质的组成是正确解答本题的关键.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案化学兴趣小组的同学发现实验室有一瓶失去标签的黑色粉末,可能是炭粉、铁粉、二氧化锰或氧化铜中的一种,为了探究其成分,同学们设计了如下实验方案:
(1)实验:
步骤 | 操作 | 现象 | 结论 |
① | 取少量粉末放在燃烧匙中,放在酒精灯火焰上灼烧。罩上内壁附有石灰水的烧杯。 | 若烧杯内壁的石灰水 ____________________ | 则粉末为炭粉 |
② | 取少量粉末于试管中,滴入足量稀硫酸。 | 将燃着的木条放在试管口,若有尖锐的爆鸣声。 | a.则粉末为____。 |
b.若黑色固体消失,_______ | 则粉末为氧化铜。 | ||
③ | 取少量固体于试管中,滴入5%的过氧化氢溶液,将带火星的木条伸入试管中。 | 若产生大量气泡,且 ___________________ | 则粉末为______。 |
(2)表达:
步骤①的化学方程式_____________________________、________________________。
步骤③的化学方程式_______________________________________________________。
(3)拓展:老师指出,步骤①不严密,你认为原因是:________________________。
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量的两种无色液体分别加入A、B两个试管中; ② 分别向A、B两试管中加入等质量的二氧化锰 | A试管中 无明显现象 B试管中试管中有气泡产生 | A试管中的无色液体是: 水;B试管中的无色液体是: 过氧化氢溶液 |
(2)如何验证B试管中产生的气体(写出操作步骤、实验现象和结论)?
将带火星的木条伸进试管内,木条复燃,说明生成的是氧气.
| A. | Y2X3 | B. | X3Y2 | C. | XY2 | D. | Y2X |
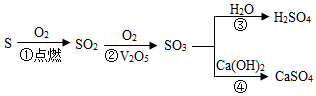 含硫元素物质间发生转化:其中硫元素化合价发生变化的是( )
含硫元素物质间发生转化:其中硫元素化合价发生变化的是( )| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
 下表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )
下表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )| 编 号 | 甲 | 乙 | 丙 | 丁 |
| A | Cu | CuO | CuSO4 | Cu(NO3)2 |
| B | Na2CO3 | NaOH | NaHCO3 | CO2 |
| C | CaCO3 | CaO | CaCl2 | Ca(NO3)2 |
| D | C | CO | CO2 | K2CO3 |
| A. | A | B. | B | C. | C | D. | D |
| 实验内容 | 主要实验现象 | 化学方程式 |
| 在盛有硝酸银溶液的试管中,插入一根洁净的铜丝 | 铜丝的表面出现银白色物质,溶液变为蓝色 | Cu+2AgNO3═Cu(NO3)2+2Ag |
| 向硝酸银溶液中滴加稀盐酸 | 有白色沉淀生成 | HCl+AgNO3═AgCl↓+HNO3 |
| 将生锈的铁钉放入稀盐酸中 | 铁锈消失,溶液变为黄色 | Fe2O3+6HCl═2FeCl3+3H2O |
| A. | 蜡烛熔化 | B. | 空气液化制氧气 | ||
| C. | 铜器在潮湿的空气中产生铜绿 | D. | 利用干冰进行人工降雨 |
| A. | 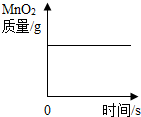 向MnO2中加入过氧化氢溶液 | B. | 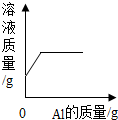 向CuSO4溶液中加入Al | ||
| C. | 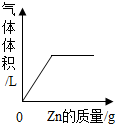 向稀盐酸中加入Zn | D. | 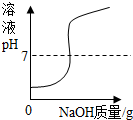 向稀盐酸中加入NaOH溶液 |