题目内容
1.小林同学用加热氯酸钾(KClO3)和二氧化锰的固体混合物的方法制取氧气,并回收催化剂二氧化锰和产物氯化钾,请你协助他.(1)制取氧气,请根据如图1回答问题:
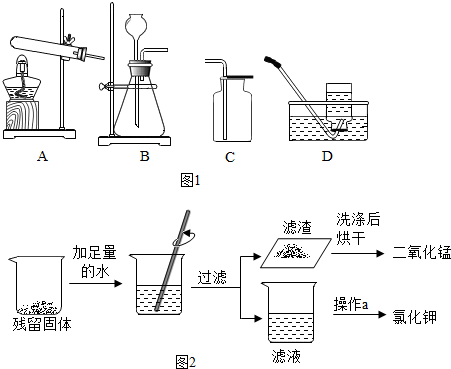
①写出装置A中的一种玻璃仪器的名称:酒精灯.
②小林同学应选用的发生装置是A(填标号),写出有关反应的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
③用C装置收集氧气,验满的方法是将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了,用D装置收集氧气,当导管口开始有气泡冒出时,不能立即收集,原因是因为装置中有空气.
(2)回收二氧化锰二氯化钾,将氯化钾和二氧化锰混合加热后的残留固体按如图2所示实验操作流程回收难溶性二氧化锰和可溶性氯化钾,请回答:
①残留固体中加水后,搅拌的目的是加快氯化钾的溶解,操作a是加热蒸发(填操作名称).
②实际回收的氯化钾的质量比理论值低,原因可能是在蒸发的过程中,有少部分氯化钾残留到蒸发皿中.
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.用C装置收集氧气,验满的方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;用D装置收集氧气,当导管口开始有气泡冒出时,不能立即收集,原因是因为装置中有空气.残留固体中加水后,搅拌的目的是加快氯化钾的溶解,操作a是加热蒸发;实际回收的氯化钾的质量比理论值低,原因可能是:在蒸发的过程中,有少部分氯化钾残留到蒸发皿中.
解答 解:(1)酒精灯是常用的加热仪器,如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;用C装置收集氧气,验满的方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;用D装置收集氧气,当导管口开始有气泡冒出时,不能立即收集,原因是因为装置中有空气;故答案为:①酒精灯;②A;2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;③将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;
(2)残留固体中加水后,搅拌的目的是加快氯化钾的溶解,操作a是加热蒸发;实际回收的氯化钾的质量比理论值低,原因可能是:在蒸发的过程中,有少部分氯化钾残留到蒸发皿中;故答案为:①加快氯化钾的溶解;加热蒸发;②在蒸发的过程中,有少部分氯化钾残留到蒸发皿中;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的验满等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. | 原子 | B. | 离子 | C. | 分子 | D. | 元素 |
| A. | K2MnO4:高锰酸钾 | B. | 2N:1个氮分子 | C. | S2-:1个硫离子 | D. | H2:2个氢原子 |
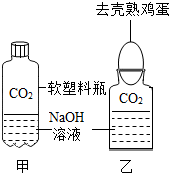 化学复习课上,老师将CO2分别通入澄清的石灰水和NaOH溶液中,我们观察到前者变浑浊,后者无明显现象.CO2和NaOH是否确实发生了化学反应?
化学复习课上,老师将CO2分别通入澄清的石灰水和NaOH溶液中,我们观察到前者变浑浊,后者无明显现象.CO2和NaOH是否确实发生了化学反应?①第一兴趣小组设计了甲、乙两个实验装置来验证,如图所示,实验现象为:
甲--软塑料瓶变瘪,乙--“瓶吞鸡蛋”
小王同学认为上述实验是可行的,其共同原理都是在密闭的体系里消耗CO2,使气体压强减小,从而观察到明显现象.
小红同学提出了质疑,他认为实验还不足以证明CO2与NaOH确实发生了反应,其理由是NaOH溶液中有水,CO2又能溶于水,究竟是CO2溶于水使气压减小的结果,还是CO2与NaOH反应使气压减小的结果,还不得而知.对小红提出的观点,你评价是正确(填“正确”或“不妥”).
小陆思考后,又补充了一个实验来回答,这个实验是:取一个与甲装置同样大小和质地的软塑料瓶,充满CO2后,注入与NaOH溶液体积相同的水,振荡,认为比较瓶子变瘪的程度即可判断.对小陆的做法,你评价是正确(填“正确”或“不妥”).
②第二兴趣小组另外设计了如下两种不同原理的实验方案,请完成如表:
| 实验步骤 | 实验现象 | 实验结论 | |
| 方法1 | 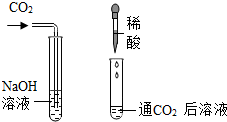 | 有产生 | CO2与NaOH确实发生了化学反应 |
| 方法2 | 将CO2通入NaOH溶液后,再向溶液中滴加溶液. | 出现 |
③由此实验探究,你得到的启示是:对于无明显现象的化学反应,可通过改变实验装置,创新的情境来观察明显的反应现象判断反应的发生.
| A. | 冬天用炭火盆取暖要注意关闭门窗 | B. | 自行车链条抹油能防止生锈 | ||
| C. | 钻石项链不能放到火上灼烧 | D. | 菜汤太咸了可以适当加些水 |
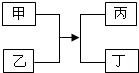 甲乙丙丁四种物质的转化关系如图所示.下列说法正确的是( )
甲乙丙丁四种物质的转化关系如图所示.下列说法正确的是( )| A. | 若丙为沉淀,则甲、乙中一定有一种物质是碱 | |
| B. | 若甲、丁为单质,则该反应一定是置换反应 | |
| C. | 若丁为水,则该反应一定是复分解反应 | |
| D. | 若丙为气体,则甲、乙中一定有单质 |
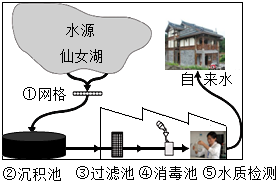 我市自来水的处理过程如图所示:
我市自来水的处理过程如图所示: