题目内容
元素周期表是化学学习的重要工具,依据如图回答问题:
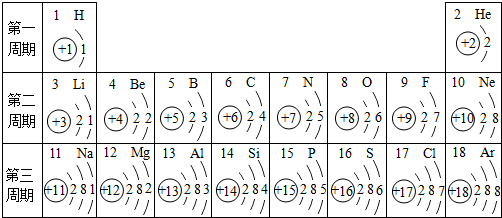
(1)图中14号元素属于 (填“金属”或“非金属”)元素,该元素的化学性质与 元素相似,即在常温下具有 性.
(2)通过如图的分析可知:元素所在的周期数= ,元素所在的族数=该元素原子的最外层电子数.
(3)根据如图中原子核外电子排布规律,原子序数为19的钾元素的原子结构示意图为 ,钾元素的原子在化学反应中容易形成离子,该离子符号是 .

(1)图中14号元素属于
(2)通过如图的分析可知:元素所在的周期数=
(3)根据如图中原子核外电子排布规律,原子序数为19的钾元素的原子结构示意图为
考点:元素周期表的特点及其应用,原子结构示意图与离子结构示意图
专题:化学用语和质量守恒定律
分析:(1)根据汉字偏旁可判断元素类别,最外层电子数决定元素化学性质;
(2)根据元素周期表进行分析;
(3)根据元素周期表和离子符号的写法进行分析.
(2)根据元素周期表进行分析;
(3)根据元素周期表和离子符号的写法进行分析.
解答:解:(1)14号元素是硅,硅元素带石字旁,是非金属元素;最外层电子数决定元素的化学性质,最外层电子数相同的元素,化学性质相似,硅元素原子最外层电子数为4,碳元素原子最外层电子数为4,因此硅、碳元素的化学性质相似,常温下也具有稳定性;
故答案为:非金属;碳;稳定;
(2)通过上表的分析可知:元素所在的周期数=元素原子的电子层数,元素所在的族数=该元素原子的最外层电子数;
故答案为:该元素原子核外的电子层数;
(3)根据上表中原子核外电子排布规律,原子序数为19的钾元素在第四周期、第一主族,应有4个电子层,最外层电子数是1,因此钾原子结构示意图为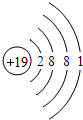 ;钾元素的原子最外层有一个电子,在化学反应中容易失去1个电子形成阳离子,该离子符号是K+.
;钾元素的原子最外层有一个电子,在化学反应中容易失去1个电子形成阳离子,该离子符号是K+.
故答案为: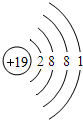 ;K+.
;K+.
故答案为:非金属;碳;稳定;
(2)通过上表的分析可知:元素所在的周期数=元素原子的电子层数,元素所在的族数=该元素原子的最外层电子数;
故答案为:该元素原子核外的电子层数;
(3)根据上表中原子核外电子排布规律,原子序数为19的钾元素在第四周期、第一主族,应有4个电子层,最外层电子数是1,因此钾原子结构示意图为
 ;钾元素的原子最外层有一个电子,在化学反应中容易失去1个电子形成阳离子,该离子符号是K+.
;钾元素的原子最外层有一个电子,在化学反应中容易失去1个电子形成阳离子,该离子符号是K+.故答案为:
 ;K+.
;K+.点评:本题主要考查元素周期表的结构、元素周期律等知识,要求学生掌握原子结构示意图的画法以及原子得失电子的判断方法.

练习册系列答案
相关题目
岳西县来榜镇是华东地区最大的瓜蒌生产基地,瓜蒌的果实、果皮、果仁(籽)、根茎均为上好的中药材.瓜蒌籽中富含维生素,其中维生素C[C6H8O6]的含量较高,下列关于维生素C的说法错误的是( )
| A、维生素C由碳、氢、氧三种元素组成 |
| B、维生素C中碳、氢、氧的原子个数比为3:4:3 |
| C、维生素C的相对分子质量为176 |
| D、维生素C中碳、氢、氧三种元素的质量比为12:1:16 |
化学上把同种元素组成的不同单质叫做同素异形体,如金刚石与石墨.下列各组物质互为同素异形体的是( )
| A、CO与CO2 |
| B、氧气与臭氧 |
| C、水与双氧水 |
| D、液氧与氧气 |
下列说法错误的是( )
| 事实 | 解释 | |
| A | 墙内开花墙外香 | 分子在不断地运动 |
| B | H2O2能杀菌消毒,而H2O不能 | 两种物质的分子构成不同 |
| C | 温度计中的水银热胀冷缩 | 原子的大小发生改变 |
| D | 50mL水与50mL酒精混合后总体积小于100mL | 分子间有间隔 |
| A、A | B、B | C、C | D、D |
有X、Y、Z三种金属,只有Z在自然界中主要以单质形式存在,如果把Y加入X的硝酸盐溶液中,Y表面有X析出.据此判断这三种金属的活动性由强到弱的顺序为( )
| A、X>Y>Z |
| B、X>Y>Z |
| C、Y>X>Z |
| D、Z>Y>X |
 已知A、B、C、D、E、F为常见物质,其中A、B含有相同的元素,B、E为氧化物,C、D、F都为单质.且F为红色,它们相互转化的关系如图所示(图中反应条件略去).
已知A、B、C、D、E、F为常见物质,其中A、B含有相同的元素,B、E为氧化物,C、D、F都为单质.且F为红色,它们相互转化的关系如图所示(图中反应条件略去).