题目内容
18.如图中A、B、C、D是四种粒子的结构示意图,请回答下列问题: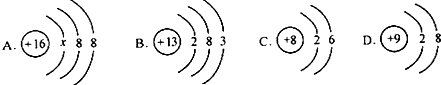
(1)A中x=2;A粒子用化学用语可表示为:S2-;
(2)由B粒子的结构示意图可知,B粒子在化学反应中易失(填得或失)电子
(3)以上四种结构示意图所表示的粒子中,表示离子的是AD(填字母代号)
分析 (1)根据原子核外电子排布规律及原子中质子数=核外电子数,进行计算解答;
(2)若最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子;
(3)根据阴离子的质子数<电子数,阳离子的质子数>电子数来分析解答.
解答 解:
(1)根据原子核外电子排布规律结合图形可知:第一层为2个电子,故x=2,A中质子数<核外电子数,为硫离子,用化学用语可表示为:S2-;
(2)由B原子结构示意图为可以看出:最外层弧线上的数字是2,最外层电子数是2,在化学反应中易失去2个电子而形成阳离子.
(3)A中的质子数=16<电子数=18,故为阴离子;D中的质子数=9<电子数=10,故为阴离子.
故答案为:
(1)2;S2-;(2)失;(3)AD.
点评 本题难度不大,考查学生对粒子结构示意图及其意义的理解,了解粒子结构示意图的意义、化学式的书写等知识是正确解题的关键.

练习册系列答案
相关题目
4.下列有关物质的性质和用途描述不正确的是( )
| A. | 钨的熔点高,可以用来制作保险丝 | |
| B. | 不锈钢抗锈性能好,可用于作外科手术刀 | |
| C. | 石灰石在高温作用下分解,可用于制备生石灰 | |
| D. | 一氧化碳气体具有可燃性,可用于作气体燃料 |
5.携手“六城”同创,共建山青水绿、天蓝地净的美丽恩施.从化学的视角你认为下列不符合该主题的是( )
| A. | 绿化、亮化、美化环境 | B. | 必要时对私家车限行 | ||
| C. | 开发和利用新能源 | D. | 生活污水直排江河 |
6.某兴趣小组对“铁锈(Fe2O3)与盐酸反应快慢的影响因素”进行了探究.
【提出问题】铁锈与盐酸反应的快慢受哪些因速的影响呢?
【猜想与假设】a.可能与盐酸的质量分数有关;
b.可能与反应的温度有关.
【设计实验】用相同质量的铁锈和足量的盐酸进行如表实验.
(1)写出铁锈与盐酸反应的化学方程式Fe2O3+6HCl═2FeCl3+3H2O.
(2)要比较温度对反应快慢的影响,应选择的实验编号是②③.
【得出结论】(3)从以上实验中可得出的结论是①温度越高,反应时间越短,反应速率越快;②酸的溶质质量分数越大,反应速率越快.
【实验拓展】(4)随后在铁锈与盐酸反应的试管中加入少量硫酸,发现反应明显加快,可能是硫酸中H+(填化学符号)加快了反应的速率,请设计一个合理的实验来验证你的假设在铁锈与盐酸反应的试管中加入少量硫酸钠溶液,发现反应速率没有改变,说明不是其中的硫酸根离子所起的作用.
(5)铁锈与盐酸反应的快慢可能还受哪些因速影响?设计实验验证.
【提出问题】铁锈与盐酸反应的快慢受哪些因速的影响呢?
【猜想与假设】a.可能与盐酸的质量分数有关;
b.可能与反应的温度有关.
【设计实验】用相同质量的铁锈和足量的盐酸进行如表实验.
| 实验编号 | 盐酸的质量分数 | 反应的速度 | 铁锈消失的时间 |
| ① | 6% | 20℃ | 240 s |
| ② | 10% | 20℃ | 115 s |
| ③ | 10% | 30℃ | 75 s |
(2)要比较温度对反应快慢的影响,应选择的实验编号是②③.
【得出结论】(3)从以上实验中可得出的结论是①温度越高,反应时间越短,反应速率越快;②酸的溶质质量分数越大,反应速率越快.
【实验拓展】(4)随后在铁锈与盐酸反应的试管中加入少量硫酸,发现反应明显加快,可能是硫酸中H+(填化学符号)加快了反应的速率,请设计一个合理的实验来验证你的假设在铁锈与盐酸反应的试管中加入少量硫酸钠溶液,发现反应速率没有改变,说明不是其中的硫酸根离子所起的作用.
(5)铁锈与盐酸反应的快慢可能还受哪些因速影响?设计实验验证.
3.如图为某化学反应的微观示意图,其中不同的球代表不同种原子.下列说法中正确的是( )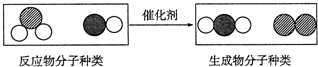

| A. | 此反应属于置换反应 | |
| B. | 化学反应前后分子的种类没有改变 | |
| C. | 原子在化学变化中可分 | |
| D. | 参加反应的两种分子的个数比为1:2 |
10.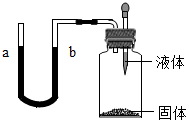 用如图所示的密闭实验装置,当胶头滴管内的液体滴下与固体接触时,液面a比液b高,但过一段时间U型管内的液面又回到持平的一组固体和液体组合是( )
用如图所示的密闭实验装置,当胶头滴管内的液体滴下与固体接触时,液面a比液b高,但过一段时间U型管内的液面又回到持平的一组固体和液体组合是( )
 用如图所示的密闭实验装置,当胶头滴管内的液体滴下与固体接触时,液面a比液b高,但过一段时间U型管内的液面又回到持平的一组固体和液体组合是( )
用如图所示的密闭实验装置,当胶头滴管内的液体滴下与固体接触时,液面a比液b高,但过一段时间U型管内的液面又回到持平的一组固体和液体组合是( )| A. | 食盐和水 | B. | 石灰石和稀盐酸 | ||
| C. | 固体氢氧化钠和水 | D. | 硝酸铵和水 |
7.三氧化二锑(Sb2O3)能与过氧化氢发生如下反应:Sb2O3+2H2O2═X+2H2O,则X的化学式为( )
| A. | Sb2O | B. | SbO3 | C. | Sb2O3 | D. | Sb2O5 |
8.(1)请在表中填入一种相应的物质的化学式:
(2)用上表的四种具体物质为反应物,写出两个它们之间相互反应的化学方程式:
①Fe+2HCl=FeCl2+H2↑;②HCl+NaOH=NaCl+H2O.
| 类别 | 单质 | 酸 | 碱 | 盐 |
| 化学式 |
①Fe+2HCl=FeCl2+H2↑;②HCl+NaOH=NaCl+H2O.
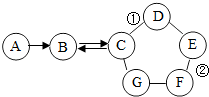 如图表示的是物质A~G相互间的关系“→”表示物质间存在的转化关系,“-”表示两端的物质能发生化学反应).相关信息如下:A、F都是单质,F是使用最多的金属材料,B是导致温室效应的主要气体之一,C在工业上广泛用于玻璃、造纸和洗涤剂的生产等,E是一种蓝色溶液.
如图表示的是物质A~G相互间的关系“→”表示物质间存在的转化关系,“-”表示两端的物质能发生化学反应).相关信息如下:A、F都是单质,F是使用最多的金属材料,B是导致温室效应的主要气体之一,C在工业上广泛用于玻璃、造纸和洗涤剂的生产等,E是一种蓝色溶液.