题目内容
10.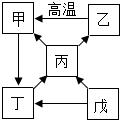 甲~戊五种物质的转化关系如图所示,已知甲是空气中的一种成分,溶于水后能使石蕊试液变红;戊与水的元素组成相同,原子个数之比为1:1.(部分反应物、产物及反应条件已略去,“→”表示物质之间能发生转化)
甲~戊五种物质的转化关系如图所示,已知甲是空气中的一种成分,溶于水后能使石蕊试液变红;戊与水的元素组成相同,原子个数之比为1:1.(部分反应物、产物及反应条件已略去,“→”表示物质之间能发生转化)(1)丙的化学式O2;
(2)乙可能为CO(填一种物质的化学式);
(3)丁→丙反应属于基本反应类型中的分解反应;
(4)甲→丁反应的化学方程式是CO2+Ca(OH)2═CaCO3↓+H2O.
分析 根据“甲是空气中的一种成分,溶于水后能使石蕊试液变红”,所以甲是二氧化碳,根据“戊与水的元素组成相同,原子个数之比为1:1”,则推测戊为双氧水,结合图框,推测乙可能为一氧化碳、氧化铁等,丙为氧气,丁为水,然后将推出的各种物质代入转化关系中验证即可.
解答 解:根据“甲是空气中的一种成分,溶于水后能使石蕊试液变红”,所以甲是二氧化碳,根据“戊与水的元素组成相同,原子个数之比为1:1”,则推测戊为双氧水,结合图框,推测乙可能为一氧化碳、氧化铁等,丙为氧气,丁为水,然后将推出的各种物质代入转化关系中验证即可.
(1)根据分析,丙为氧气,则其化学式为O2;
(2)根据分析,乙可能为一氧化碳、氧化铁、氧化铜等,故CO;
(3)丁→丙反应,即为水通电分解生成氢气和氧气,故属于基本反应类型中的分解反应;
(4)甲→丁反应,即二氧化碳与氢氧化钙反应生成碳酸钙和水,故其化学方程式是CO2+Ca(OH)2═CaCO3↓+H2O.
故答案为:
(1)O2;(2)CO;(3)分解反应;(4)CO2+Ca(OH)2═CaCO3↓+H2O.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
20.Ca2+和Ca两种粒子具有相同的是( )
| A. | 电子数 | B. | 质子数 | C. | 化学性质 | D. | 最外层电子数 |
1.关于分子、原子、离子的说法,其中正确的是( )
| A. | 原子是最小的微粒,不可再分 | |
| B. | 在化学变化中,物质的分子不会改变 | |
| C. | 当水变成水蒸气时,水分子间隔变小 | |
| D. | 分子、原子、离子都可以直接构成物质 |
5.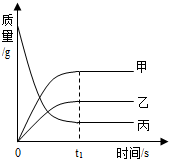 如图反映了某个化学反应各物质质量与时间的关系,下列描述正确的是( )
如图反映了某个化学反应各物质质量与时间的关系,下列描述正确的是( )
 如图反映了某个化学反应各物质质量与时间的关系,下列描述正确的是( )
如图反映了某个化学反应各物质质量与时间的关系,下列描述正确的是( )| A. | 该反应是化合反应 | |
| B. | 甲的相对分子质量大于乙 | |
| C. | 该反应的生成物只有一种 | |
| D. | t时,参加反应的丙的质量一定等于甲、乙的质量之和 |
15.分析推理是化学学习中常用的思维方法,下列说法正确的是( )
| A. | 分子和原子都是不带电的粒子,所以不带电的粒子一定是分子或原子 | |
| B. | 离子都带有一定量的电荷,带电荷的粒子一定是离子 | |
| C. | 铜具有良好导电性可作导线,能作导线的材料一定具有导电性 | |
| D. | 单质中只含有一种元素,所以由一种元素组成的物质一定是单质 |
19.小华同学用60克氯酸钾和二氧化锰的混合固体进行加热制氧气,测得反应后剩余固体的质量(m)与反应时间(min)关系如表:
请回答下列问题(1)分析表中记录的数据,当氯酸钾充分反应后,生成氧气的质量为16克;
(2)在氯酸钾中,钾元素与氧元素的质量比为13:16;
(3)求原混合固体中氯酸钾的质量,并写出计算过程;
(4)求60克氯酸钾和二氧化锰的混合物中二氧化锰的质量分数,并写出计算过程.
| 反应时间min | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 反应后固体的质量g | 60 | 56.8 | 53.6 | 50.4 | 47.2 | 44 | 44 | 44 |
(2)在氯酸钾中,钾元素与氧元素的质量比为13:16;
(3)求原混合固体中氯酸钾的质量,并写出计算过程;
(4)求60克氯酸钾和二氧化锰的混合物中二氧化锰的质量分数,并写出计算过程.