题目内容
甲同学为区别氢氧化钠和氢氧化钙溶液,设计如图所示的四组实验方案.
(1)其中能达到实验目的方案是 (填字母);
(2)在C组实验中发生的化学方程式为 ;
(3)实验结束后,甲同学将A、C组四支试管中的溶液倒入同一容器中,看到溶液变浑浊,该现象说明有 (填化学式)物质生成,滴入酚酞后溶液呈红色,说明此混合溶液呈 性;
(4)属于碱的共同性质的方案是 (填字母).

(1)其中能达到实验目的方案是
(2)在C组实验中发生的化学方程式为
(3)实验结束后,甲同学将A、C组四支试管中的溶液倒入同一容器中,看到溶液变浑浊,该现象说明有
(4)属于碱的共同性质的方案是
考点:碱的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的碱 碱的通性
分析:(1)根据氢氧化钠和氢氧化钙的性质可以知道,它们都能够和稀盐酸反应且都没有现象,都能使酚酞变红,氢氧化钠不能和碳酸钠反应,但是氢氧化钙可以和碳酸钠反应生成白色沉淀,氢氧化钠和氢氧化钙都能和二氧化碳反应,但是氢氧化钠和二氧化碳反应没有现象,而氢氧化钙和二氧化碳反应生成白色沉淀,可以据此解答该题;
(2)C组中发生的反应为氢氧化钙和碳酸钠的反应,该反应生成了碳酸钙沉淀和氢氧化钠,可以据此写出该反应的化学方程式;
(3)根据题意生成的白色沉淀只能是碳酸钙,可以据此解答该题;
(4)碱的共性有:①能使指示剂酚酞变红,②能与酸发生中和反应,③能与非金属氧化物二氧化碳反应,④能与某些盐反应;
(2)C组中发生的反应为氢氧化钙和碳酸钠的反应,该反应生成了碳酸钙沉淀和氢氧化钠,可以据此写出该反应的化学方程式;
(3)根据题意生成的白色沉淀只能是碳酸钙,可以据此解答该题;
(4)碱的共性有:①能使指示剂酚酞变红,②能与酸发生中和反应,③能与非金属氧化物二氧化碳反应,④能与某些盐反应;
解答:解:(1)根据氢氧化钠和氢氧化钙的性质可以知道,它们都能够和稀盐酸反应且都没有现象,都能使酚酞变红,氢氧化钠不能和碳酸钠反应,但是氢氧化钙可以和碳酸钠反应生成白色沉淀,氢氧化钠和氢氧化钙都能二氧化碳反应,但是氢氧化钠反应没有现象,和氢氧化钙反应生成白色沉淀,所以能够实现目的实验为C和D;
(2)C组中发生的反应为氢氧化钙和碳酸钠的反应,该反应生成了碳酸钙沉淀和氢氧化钠,该反应的化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(3)根据题意生成的白色沉淀只能是碳酸钙,其化学式为:CaCO3;滴入酚酞后溶液呈红色,说明此混合溶液呈碱性.
(4)与盐酸、二氧化碳、酚酞反应属于碱的共同性质,碳酸钠不能与氢氧化钠反应;
答案
(1)C、D (2)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
(3)CaCO3;碱 (4)ABD
(2)C组中发生的反应为氢氧化钙和碳酸钠的反应,该反应生成了碳酸钙沉淀和氢氧化钠,该反应的化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(3)根据题意生成的白色沉淀只能是碳酸钙,其化学式为:CaCO3;滴入酚酞后溶液呈红色,说明此混合溶液呈碱性.
(4)与盐酸、二氧化碳、酚酞反应属于碱的共同性质,碳酸钠不能与氢氧化钠反应;
答案
(1)C、D (2)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
(3)CaCO3;碱 (4)ABD
点评:要想解答好这类题目,首先,要理解和熟记碱的化学性质、用途、反应现象和化学方程式,以及与之相关的知识.然后,根据所给的实验、问题情景,结合所学的相关知识和技能,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

练习册系列答案
相关题目
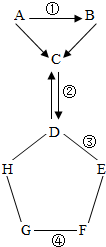 整理、归纳物质性质之间的相互联系,是化学学习的一种有效方法.如图表示的是常见物质A-H相互间的常见关系(“→”表示物质间的转化关系,“--”表示两端的物质能发生化学反应).A、G都是单质,气体C常用于灭火,F是一种蓝色溶液,可用于配制农药波尔多液.以下正确的是( )
整理、归纳物质性质之间的相互联系,是化学学习的一种有效方法.如图表示的是常见物质A-H相互间的常见关系(“→”表示物质间的转化关系,“--”表示两端的物质能发生化学反应).A、G都是单质,气体C常用于灭火,F是一种蓝色溶液,可用于配制农药波尔多液.以下正确的是( )| A、物质A一定是碳单质,物质C是CO2 |
| B、物质H、E可能是不同类型的物质 |
| C、物质D可能是CaCO3,物质G可能是Fe |
| D、①②③④物质间的转化、或发生化学反应时可涉及到所有基本反应类型 |
银、铁、铜是日常生活中经常接触到的三种金属.对Ag、Fe、Cu三种金属活动性顺序进行探究时,下列所选试剂组不可行的是( )
| A、Fe、Ag、CuSO4溶液 |
| B、Cu、FeSO4溶液、AgNO3溶液 |
| C、Cu、Ag、FeSO4溶液 |
| D、Fe、Cu、稀盐酸、AgNO3溶液 |
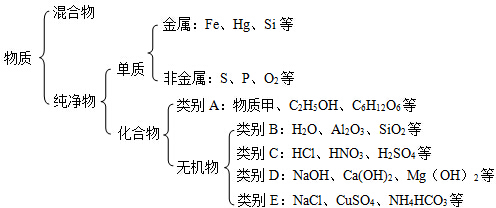
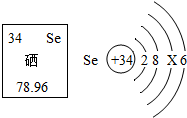 紫薯中除含淀粉、蛋白质、多种维生素外,还富含花青素和硒元素.其中硒元素的部分信息如图所示:
紫薯中除含淀粉、蛋白质、多种维生素外,还富含花青素和硒元素.其中硒元素的部分信息如图所示: