题目内容
18.大多数花卉喜欢微酸性土壤.某花卉长势不佳,经测定盆中土壤pH为8.2,在施用较稀FeSO4溶液浇灌后长势良好,这说明FeSO4溶液显酸(填“酸”“碱”或“中”)性;Al与NaOH溶液反应会生成H2和Na[Al(OH)4],该反应的化学方程式为2NaOH+2Al+6H2O═2Na[Al(OH)4]+3H2↑.分析 该花长势不佳,土壤的pH为8.2,为碱性,用较稀的硫酸亚铁溶液浇灌后,长势良好,根据酸碱相互反应的性质,说明所施该溶液为酸性.根据反应物、生成物和条件书写方程式.
解答 解:该花长势不佳,土壤的pH为8.2,为碱性,用较稀的硫酸亚铁溶液浇灌后,长势良好,根据酸碱相互反应的性质,说明所施该溶液为酸性.
Al与NaOH溶液反应产生了氢气的同时还生成了Na[Al(OH)4],写出该反应的化学方程式:2NaOH+2Al+6H2O=2Na[Al(OH)4]+3H2↑.
故答案为:酸;2NaOH+2Al+6H2O═2Na[Al(OH)4]+3H2↑.
点评 本题考查了溶液的酸碱性与农作物的生长关系,完成此题,可以依据题干提供的信息结合已有的知识进行.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
8.下列说法正确的是( )
| A. | 用食盐腌制鱼,肉等食品 | B. | 用甲醛溶液浸泡海产品 | ||
| C. | 农业上提倡大量施用农药 | D. | 造成酸雨的主要气体是CO2 |
9.下列化学用语表达的意义正确的是( )
| A. | 2O2-2个氧分子 | B. | Fe2+-1个铁离子 | C. | 2个氢原子-H2 | D. | 氮原子-N2 |
6.2015年12月15日“上合会议”在郑州召开,为摆脱雾霾,出现“上合蓝”,下列哪些做法是不可行的( )
| A. | 减少用电 | B. | 绿色排放 | ||
| C. | 节俭生活 | D. | 工厂尾气不经处理,直接排放 |
13.向一定量的NaCl溶液中加入足量的AgNO3溶液,充分反应后过滤,所得沉淀质量恰好等于原NaCl溶液质量.则原NaCl溶液中溶质的质量分数约为( )
| A. | 50% | B. | 20% | C. | 10% | D. | 40.8% |
10.下列实验操作错误的是( )
| A. | 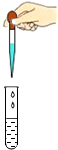 滴加液体 | B. | 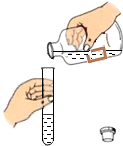 倾倒液体 | ||
| C. | 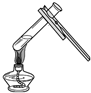 加热液体 | D. | 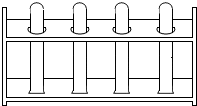 放置洗净的试管 |

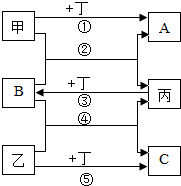 如图所示:甲、乙、丙、丁各是一种单质;A、B、C是氧化物,C中两种元素质量之比为3﹕8;丙是一种紫红色金属.图中“-”表示两端的物质问能发生化学反应;“→”表示物质间存在转化关系.
如图所示:甲、乙、丙、丁各是一种单质;A、B、C是氧化物,C中两种元素质量之比为3﹕8;丙是一种紫红色金属.图中“-”表示两端的物质问能发生化学反应;“→”表示物质间存在转化关系.