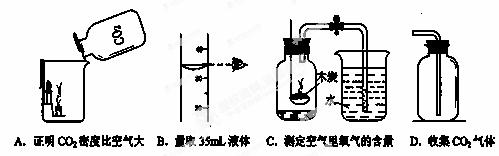
题目内容
向某铁粉样品中,加入溶质质量分数为10%的硫酸铜溶液160 g,恰好完全反应,样品中杂质不溶于水也不与硫酸铜反应。请结合下图提供的数据计算。
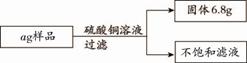 |
(1)a的数值。
(2)向不饱和滤液中加入40 .8 g水,求所得溶液中溶质的质量分数。
.8 g水,求所得溶液中溶质的质量分数。
【解】 设:样品中铁的质量为x,生成铜的质量为y,生成硫酸亚铁的质量为z
设:样品中铁的质量为x,生成铜的质量为y,生成硫酸亚铁的质量为z
Fe + CuSO4 = FeSO4 + Cu
56 160 152 64
x 160g×10% z y
x = 5.6g y = 6.4g z = 15.2g ···························1 分
(1)a = 5.6g +(6.8g – 6.4g)= 6g ····························1 分
(2)5.6g + 160g – 6.4g + 40.8g = 200g
15.2g / 200g × 100% = 7.6% ···························1 分
答:略。

练习册系列答案
相关题目
下列做法,对保护环境不利的是( )
|
| A. | 开发推广氢能汽车 | B. | 汽车限购限行 |
|
| C. | 燃放烟花爆竹增强节日气氛 | D. | 用天然气代替燃煤供暖 |



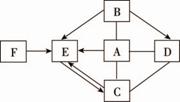 (4)已知上述物质间存在右图所示的关系
(4)已知上述物质间存在右图所示的关系 ①浓硫酸和水 ②镁和稀盐酸
①浓硫酸和水 ②镁和稀盐酸 氧化钠固体和水 ⑥碳酸氢钠和稀盐酸
氧化钠固体和水 ⑥碳酸氢钠和稀盐酸 是在汽油中加入适量的乙醇混合而成的一种燃料。下列叙述正确的是( )A.乙醇汽油是一种新型化合物 B.用玉米、高粱发酵可以制得乙醇汽油
是在汽油中加入适量的乙醇混合而成的一种燃料。下列叙述正确的是( )A.乙醇汽油是一种新型化合物 B.用玉米、高粱发酵可以制得乙醇汽油 D.汽车使用乙醇汽油能减少有害气体排放
D.汽车使用乙醇汽油能减少有害气体排放



 C D
C D