题目内容
有8gCO与CO2混合气体已知其中碳元素质量分数为30%,将该混合气体通过灼热CuO后,再将余下气体通往足量石灰水,最多可得到白色沉淀的质量是( )
| A、28.6g | B、23.7g |
| C、20g | D、18.2g |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:由于CO能与氧化铜反应而变成二氧化碳,该混合气体通过灼热氧化铜后,全部转化为二氧化碳,二氧化碳与石灰水反应形成碳酸钙沉淀,根据化学变化前后元素质量不变,所得碳酸钙中碳元素即原混合气体中碳元素,根据碳元素质量可计算形成沉淀碳酸钙的质量.
解答:解:CO与CO2混合气体中所含碳元素的质量=8g×30%=2.4g,根据化学变化前后元素质量不变,即所得沉淀碳酸钙中含碳元素2.4g,
含C元素2.4g的碳酸钙的质量=2.4g÷
×100%=20g.
答案:C
含C元素2.4g的碳酸钙的质量=2.4g÷
| 12 |
| 100 |
答案:C
点评:根据化学变化前后元素质量不变,判断出所生成沉淀中所含碳元素质量即原混合气体中碳元素质量,是解答问题的关键.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
在进行化学实验探究时,认真操作、细心观察,可以培养我们严谨的科学态度.下列实验探究过程,可以明显感觉到溶于水有吸热现象的是( )
| A、食盐溶于水 |
| B、硝酸铵溶于水 |
| C、生石灰与水反应 |
| D、浓硫酸溶于水 |
在2A+B═2C反应中,已知A的相对分子质量为24,C的相对分子质量为40,则B的相对分子质量为( )
| A、16 g |
| B、32 g |
| C、16 |
| D、32 |
如图所示,下列实验操作正确的是( )
A、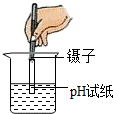 测定溶液的pH |
B、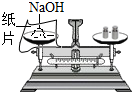 称量氢氧化钠 |
C、 稀释浓硫酸 |
D、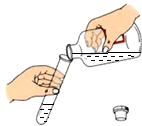 倾倒液体 倾倒液体 |
如图所示物质的用途主要利用其化学性质的是( )
A、 活性炭净水 |
B、 金属做导线 |
C、 干冰用于人工降雨 |
D、 富氧炼钢 |

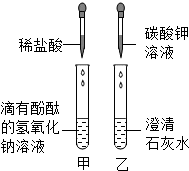 某校研究学习小组的同学在探究复分解反应发生的条件时,进行了如图所示的实验.
某校研究学习小组的同学在探究复分解反应发生的条件时,进行了如图所示的实验.