题目内容
18.甲、乙、丙三个集气瓶中,分别盛有氧气、氮气、空气中的一种,用一根燃着的木条分别伸入集气瓶中,依次观察到甲瓶火焰熄灭,乙瓶中照常燃烧,丙瓶木条燃烧火焰更大更明亮,则可推断所盛气体依次是( )| A. | 氮气、空气、氧气 | B. | 氧气、氮气、空气 | C. | 空气、氧气、氮气 | D. | 氮气、氧气、空气 |
分析 根据空气中含有21%的氧气,能支持木条的燃烧,燃着的木条放入空气中燃烧不变;氧气能支持燃烧,燃着木条放入氧气中会燃烧更旺;氮气不能燃烧、不能支持燃烧,燃着的木条放入氮气中会立即熄灭;据此进行分析判断.
解答 解:用一根燃着的小木条分别插人瓶中,根据观察到的现象:木条火焰熄灭,说明瓶内气体为氮气;木条照常燃烧,说明瓶内为空气;木条燃烧更旺,说明瓶内气体为氧气.三瓶气体中依次是氮气、空气、氧气.
故选:A.
点评 本题难度不大,考查利用燃烧的木条区分空气、氧气、氮气三种气体的方法,掌握氧气、氮气的性质是正确解答本题的关键.

练习册系列答案
相关题目
8.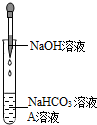 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
(1)实验装备
①查阅资料:NaHCO3+NaOH═Na2CO3+H2O
②用一定溶质的质量分数的NaHCO3、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考.
表中的现象Ⅰ为有气泡产生,现象Ⅱ对应反应的化学方程式为Ca(OH)2+Na2CO3=2NaOH+CaCO3↓.
(2)实验过程
【实验1】证明反应生成了Na2CO3
同学们选用上表实验中的药品,设计了如图所示实验,先在NaHCO3溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是CaCl2.
有同学提出这个实验不足以证明有Na2CO3生成,其理由是CaCl2 和NaOH反应生成Ca(OH)2,氢氧化钙是微溶物,在溶液中也产生沉淀.为了证明有Na2CO3生成,需要继续进行的操作是;取少量反应后滤液加入足量的稀盐酸,若产生无色气体证明有Na2CO3生成,反之则没有.
【实验2】证明反应后NaHCO3不存在
同学们参考上表中的实验,又设计了一个实验,虽然没有观察到明显的实验现象,但可以证明反应发生了,该实验方案是取少量反应后的溶液加热至沸腾,将气体通入澄清石灰水,若澄清石灰水变浑浊,证明有:NaHCO3存在,反之则没有.
(3)实验反思
通过实验1和实验2说明,对于没有明显现象的化学反应,可以从两个不同的角度证明反应的发生,这两个角度是一是可以通过检验反应物证明反应发生,二是可以通过检验产物证明反应发生.
 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.(1)实验装备
①查阅资料:NaHCO3+NaOH═Na2CO3+H2O
②用一定溶质的质量分数的NaHCO3、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考.
| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | 现象Ⅰ | 无明显变化 | 产生气泡 |
| 加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
(2)实验过程
【实验1】证明反应生成了Na2CO3
同学们选用上表实验中的药品,设计了如图所示实验,先在NaHCO3溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是CaCl2.
有同学提出这个实验不足以证明有Na2CO3生成,其理由是CaCl2 和NaOH反应生成Ca(OH)2,氢氧化钙是微溶物,在溶液中也产生沉淀.为了证明有Na2CO3生成,需要继续进行的操作是;取少量反应后滤液加入足量的稀盐酸,若产生无色气体证明有Na2CO3生成,反之则没有.
【实验2】证明反应后NaHCO3不存在
同学们参考上表中的实验,又设计了一个实验,虽然没有观察到明显的实验现象,但可以证明反应发生了,该实验方案是取少量反应后的溶液加热至沸腾,将气体通入澄清石灰水,若澄清石灰水变浑浊,证明有:NaHCO3存在,反之则没有.
(3)实验反思
通过实验1和实验2说明,对于没有明显现象的化学反应,可以从两个不同的角度证明反应的发生,这两个角度是一是可以通过检验反应物证明反应发生,二是可以通过检验产物证明反应发生.
13.下列实验操作,能达到预期目的是( )
①用托盘天平称取5.6g氧化铜粉末
②用容积为10mL的试管盛5mL水在酒精灯上加热
③用排水集气法可得到比较纯净的氧气
④用10mL量筒量取8.2mL水.
①用托盘天平称取5.6g氧化铜粉末
②用容积为10mL的试管盛5mL水在酒精灯上加热
③用排水集气法可得到比较纯净的氧气
④用10mL量筒量取8.2mL水.
| A. | 只有①④ | B. | ①②④ | C. | ①③④ | D. | 只有②③ |

