题目内容
19.下列几组物质按酸,碱,盐顺序排列的是( )| A. | HNO3,NH3•H2O,CuSO4 | B. | KNO3,NaOH,HCl | ||
| C. | H2SO4,Na2CO3,KOH | D. | Ca(OH)2,HCl,NaCl |
分析 根据酸、碱、盐的定义判断.酸是指电离时生成的阳离子全部是氢离子的化合物,碱是指电离时产生的阴离子全部是氢氧根离子的化合物,盐是指由金属离子(或铵根离子)与酸根离子构成的化合物.
解答 解:A、硝酸属于酸,氨水属于碱,硫酸铜属于盐,故A正确;
B、硝酸钾属于盐,氢氧化钠属于碱,盐酸属于酸,故B错误;
C、硫酸属于酸,碳酸钠属于盐,氢氧化钾属于碱,故C错误;
D、氢氧化钙属于碱,盐酸属于酸,氯化钠属于盐,故D错误.
故选:A.
点评 物质的分类知识是初中化学的教学难点,也是考查的热点之一,透彻理解有关概念,明确概念间的相互关系是解题的关键.

练习册系列答案
 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
9.下列各组内表示同一种物质的是( )
| A. | 冰、干冰、二氧化碳 | B. | 氢氧化钙、熟石灰、石灰石 | ||
| C. | 盐酸、氯化氢、食盐 | D. | 烧碱、火碱、氢氧化钠 |
7.某厨房清洁剂的pH大约是12-13,向其中加入酚酞试液,溶液颜色为( )
| A. | 紫色 | B. | 红色 | C. | 蓝色 | D. | 无色 |
4.活动小组同学通过Al,Fe,Cu三种金属与稀盐酸反应的实验,验证它们的活动性.
【所用药品】
溶质质量分数相同的稀盐酸,大小,形状相同的铝,铁,铜
【实验记录】
【分析与结论】
(1)实验开始时铝表面几乎无气泡产生的原因是铝表面有致密的氧化膜.
(2)铜表面始终无气泡产生的原因是铜不与酸反应(或铜在金属活动性顺序表中排在H之后).
(3)根据一段时间后三种金属与稀盐酸反应的现象,可证明三种金属的活动性由强到弱依次是Al>Fe>Cu
如图是小明配制100g溶质质量分数为12%的NaCl溶液的有关实验操作示意图.
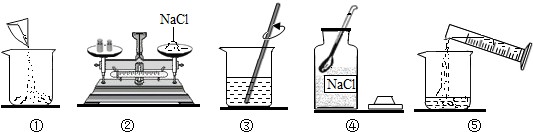
(1)配制过程中使用的四种玻璃仪器,分别是广口瓶、烧杯、玻璃棒、量筒.
(2)请你指出图中一处错误操作,并分析该操作可能造成的后果.②中物码放反了,会导致称取的氯化钠的质量减少.
(3)图②、图③表示的操作步骤分别是称量、溶解.
(4)配制时需称量氯化钠12g,如果氯化钠中含有少量不溶的杂质,溶质的质量分数会偏小(填“偏大”或“偏小”);量取水最好选择③的量筒(填序号①10mL②50mL③100mL).(水的密度为1g/cm3)
【所用药品】
溶质质量分数相同的稀盐酸,大小,形状相同的铝,铁,铜
【实验记录】
| Al | Fe | Cu | ||
| 现象 | 开始时 | 几乎无气泡产生 | 产生气泡速率慢 | 无气泡产生 |
| 一段时间后 | 产生气泡速率快 | 产生气泡速率慢 | 无气泡产生 |
(1)实验开始时铝表面几乎无气泡产生的原因是铝表面有致密的氧化膜.
(2)铜表面始终无气泡产生的原因是铜不与酸反应(或铜在金属活动性顺序表中排在H之后).
(3)根据一段时间后三种金属与稀盐酸反应的现象,可证明三种金属的活动性由强到弱依次是Al>Fe>Cu
如图是小明配制100g溶质质量分数为12%的NaCl溶液的有关实验操作示意图.

(1)配制过程中使用的四种玻璃仪器,分别是广口瓶、烧杯、玻璃棒、量筒.
(2)请你指出图中一处错误操作,并分析该操作可能造成的后果.②中物码放反了,会导致称取的氯化钠的质量减少.
(3)图②、图③表示的操作步骤分别是称量、溶解.
(4)配制时需称量氯化钠12g,如果氯化钠中含有少量不溶的杂质,溶质的质量分数会偏小(填“偏大”或“偏小”);量取水最好选择③的量筒(填序号①10mL②50mL③100mL).(水的密度为1g/cm3)
11.金属材料在生产、生活中有广泛的用途.下列有关金属的说法中不正确的是( )
| A. | 铁制品在潮湿空气中易生锈 | |
| B. | 常温下所有金属都是银白色的固体 | |
| C. | 铁和稀硫酸反应生成硫酸亚铁和氢气 | |
| D. | 合金的许多性能和组成它们的纯金属不同 |
8.要使任意一种不饱和溶液变成饱和溶液,最可靠的方法是( )
| A. | 升高温度 | B. | 降低温度 | C. | 增加溶剂 | D. | 增加溶质 |
 将等质量的X和Y两种金属粉末,分别放入相同质量分数的足量稀盐酸中,反应生成H2的质量与反应时间的关系如图所示,据图回答
将等质量的X和Y两种金属粉末,分别放入相同质量分数的足量稀盐酸中,反应生成H2的质量与反应时间的关系如图所示,据图回答 某兴趣小组要测定高锰酸钾样品的纯度(假设杂质受热不反应),请根据下列装置填空:
某兴趣小组要测定高锰酸钾样品的纯度(假设杂质受热不反应),请根据下列装置填空: