题目内容
19.为了除去食盐样品中含有的少量氯化镁和硫酸钠杂质,某科学探究小组运用所学知识设计了如下图所示①至⑤步除杂方案:
请根据上述除杂方案,回答下列问题:
(1)滤液C中的溶质有氯化钠、氢氧化钠、氯化钡;操作⑤中加入过量盐酸的作用是除去过量的碳酸钠、氢氧化钠.
(2)若在操作③中改为加过量的Ba(NO3)2溶液,固体丁中可能含有的杂质是硝酸钠.
分析 (1)根据氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,氯化钡和硫酸钠反应生成硫酸钡沉淀和氯化钠,加入的氢氧化钠、氯化钡是过量的进行分析;
根据碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,过量的氢氧化钠、碳酸钠对于氯化钠来说仍是杂质进行分析;
(2)根据硝酸钡和硫酸钠、碳酸钠反应生成硫酸钡沉淀、碳酸钡沉淀和硝酸钠进行分析.
解答 解:(1)氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,氯化钡和硫酸钠反应生成硫酸钡沉淀和氯化钠,加入的氢氧化钠、氯化钡是过量的,所以滤液C中的溶质有:氯化钠、氢氧化钠、氯化钡;碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,过量的氢氧化钠、碳酸钠对于氯化钠来说仍是杂质,所以操作⑤中加入过量盐酸的作用是:除去过量的碳酸钠、氢氧化钠;
(2)硝酸钡和硫酸钠、碳酸钠反应生成硫酸钡沉淀、碳酸钡沉淀和硝酸钠,所以在操作③中改为加过量的Ba(NO3)2溶液,固体丁中可能含有的杂质是硝酸钠.
故答案为:(1)氯化钠、氢氧化钠、氯化钡;除去过量的碳酸钠、氢氧化钠;
(2)硝酸钠.
点评 本题主要考查了依据物质的性质书写方程式的能力,及在粗盐提纯的过程中所选用除杂和净化的方法,除去杂质不要引入新的杂质,对于实验过程中过量的试剂都要除去,能很好考查学生分析、解决问题的能力.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
14.NASA近日宣布,在“伽利略”号探测器及哈勃太空望远镜传回数据的帮助下,发现木星的卫星--木卫三的冰盖下有一片咸水海洋.这片海洋存在于厚度约15万米的冰盖下,深度约为10万米,是地球海洋深度的10倍.这一发现再次为科学家拓宽视野,使探寻太阳系宜居星球的努力更进一步.水是生命之源,下列关于水的叙述不正确的是( )
| A. | 生物体内的生化反应必须在水中进行 | |
| B. | 水是由许许多多水分子构成的氧化物 | |
| C. | 水的污染会引起土壤污染 | |
| D. | 饮用蒸馏水比饮用矿泉水对身体更有益 |
4.用已知溶质质量分数的溶液可以测定未知溶液的溶质质量分数.实验室有一瓶标签模糊的稀盐酸,某同学为了测定其溶质质量分数,进行了如下实验:
①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴紫色石蕊试液(质量忽略不计),重新称量;
②往上述锥形瓶中逐滴加入溶质质量分数为16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由红色恰好变为紫色时,停止滴加,再次称量.数据如下表:
(1)若要配制500克16%的氢氧化钠溶液,需要氢氧化钠固体80克.
(2)本次实验中,实际消耗的氢氧化钠溶液质量为25克.
(3)请通过计算确定该瓶稀盐酸的溶质质量分数.
(4)另有同学做了同样的实验,却得到了不同的结果.于是用精密pH试纸测得反应后锥形瓶内溶液的pH为8.2,则他测出的盐酸溶质质量分数偏大(填“偏大”或“偏小”),造成这一偏差的原因是石蕊试液的变色不明显,你能改进这个测量过程吗?请简要描述改进方案;①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴酚酞试液(质量忽略不计),重新称量;②往上述锥形瓶中逐滴加入溶质质量分数为16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由无色恰好变为红色时,停止滴加,再次称量.
①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴紫色石蕊试液(质量忽略不计),重新称量;
②往上述锥形瓶中逐滴加入溶质质量分数为16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由红色恰好变为紫色时,停止滴加,再次称量.数据如下表:
| 锥形瓶 | 锥形瓶+稀盐酸 | 锥形瓶+反应后溶液 | |
| 质量(克) | 35.5 | 55.5 | 80.5 |
(2)本次实验中,实际消耗的氢氧化钠溶液质量为25克.
(3)请通过计算确定该瓶稀盐酸的溶质质量分数.
(4)另有同学做了同样的实验,却得到了不同的结果.于是用精密pH试纸测得反应后锥形瓶内溶液的pH为8.2,则他测出的盐酸溶质质量分数偏大(填“偏大”或“偏小”),造成这一偏差的原因是石蕊试液的变色不明显,你能改进这个测量过程吗?请简要描述改进方案;①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴酚酞试液(质量忽略不计),重新称量;②往上述锥形瓶中逐滴加入溶质质量分数为16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由无色恰好变为红色时,停止滴加,再次称量.
11.根据物质的性质,下列用途错误的是( )
| A. | 用熟石灰改良碱性土壤 | B. | 用焦炭冶炼金属 | ||
| C. | 用干冰作致冷剂保存食品 | D. | 用浓硫酸干燥二氧化碳气体 |
4.如表是三种气体的密度(在0℃、101kPa条件下测定)和溶解程度.实验室要收集二氧化硫气体,可采取的方法是( )
| 气体 性质 | 氢气 | 二氧化碳 | 二氧化硫 |
| 密度(g•L-1) | 0.08987 | 1.975 | 2.716 |
| 溶解程度 | 极难溶于水 | 能溶于水 | 易溶于水 |
| A. | 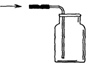 | B. | 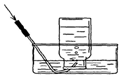 | C. |  | D. | 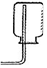 |