题目内容
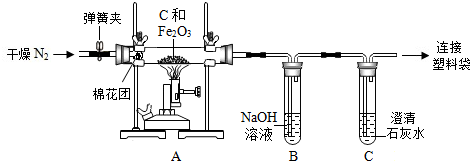
6.几年前,一辆载满20t电石的挂车,在浙江滨江区燃起熊熊大火并伴有大量黑烟.事故路面上洒落了五六百米燃着的石头.这辆货车在雨中整整燃烧了一天,消防官兵对大火也束手无措.大家对电石的化学性质产生了浓厚的兴趣,请你一起与他们完成下列探究活动.【查阅资料】电石的主要成分是碳化钙(CaC2),可以与水反应生成一种可燃性气体及白色固体.常见的可燃性气体中,乙炔(C2H2)燃烧时伴有大量黑烟.
【猜想与假设】电石与水反应生成的可燃性气体是:氧气、氢气或乙炔(C2H2);电石与水反应生成的白色固体是:氧化钙、氢氧化钙或碳酸钙.大家讨论后一致认为①该气体不可能是氧气,原因是氧气不具有可燃性,②白色固体不可能是氧化钙,原因是(用化学方程式表示)CaO+H2O═Ca(OH)2.
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取适量电石加水反应,收集生成的气体,验纯后点燃. | 气体燃烧,产生黄色火焰并伴有浓烈黑烟. | 电石与水反应产生的气体是乙炔(或C2H2) |
| (2)取适量反应后生成的固体于试管中,滴加过量稀盐酸. | 固体溶解,无气泡放出. | 电石与水反应产生的固体不是碳酸钙 |
| (3)取适量反应后生成的固体于试管中加水,向上层清液中滴加2~3滴酚酞. | 溶液变红 | 电石与水反应产生的固体是氢氧化钙 |
分析 【猜想假设】根据质量守恒定律反应前后元素的种类不变及氧气不具有可燃性进行分析;
根据氧化钙遇到水会产生氢氧化钙分析;
【实验探究】根据信息结合实验的现象分析产物的成分;根据碳酸钙和氢氧化钙的性质分析实验;
【反思交流】根据现象分析能量的变化.
解答 解:【猜想假设】由于氧气不具有可燃性,故不可能是氧气;因为氧化钙遇到水会产生氢氧化钙,所以白色固体不可能是氧化钙;
【实验探究】(1)资料中乙炔(C2H2)燃烧时伴有大量黑烟,而氢气燃烧不会产生黑烟,因此电石与水反应产生的气体是乙炔;
(2)因为结论电石与水反应产生的固体不是碳酸钙,因此加盐酸不会产生气泡;
(3)因为结论电石与水反应产生的固体是氢氧化钙,氢氧化钙的溶液呈现碱性,能够使酚酞试液变成红色;
【反思交流】根据满载电石的货车遇大雨着火的原因是电石主要成分碳化钙(CaC2)能与水反应生成可燃性气体,且该反应放热;
故答案为:【猜想假设】氧气不具有可燃性;CaO+H2O═Ca(OH)2;
【实验探究】乙炔(或C2 H2 );酚酞;
【反思交流】放热.
点评 本题属于信息题的考查,可以依据题目提供的信息结合相关的知识进行分析得出结论,难度不大.

练习册系列答案
相关题目
16.下图所示操作中,正确的是( )
| A. | 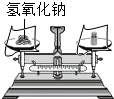 称量固体质量 | B. | 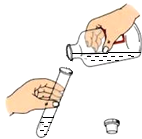 取用液体 | C. | 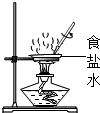 蒸发液体 蒸发液体 | D. | 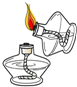 点燃酒精灯 |
1.为除去下表物质中杂质(括号内为杂质),所选试剂及操作方法均正确的是( )
| 选项 | 物质 | 所选试剂及操作方法 |
| A | Cu(CuO) | 通入氧气并加热 |
| B | NaCl液(Na2CO3) | 加入适量氯化钙溶液充分反应后过滤 |
| C | CaO(CaCO3) | 加入适量稀盐酸溶解、过滤 |
| D | CO2(HCl) | 气体通过盛有足量氢氧化钠溶液洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
18.如图是对四个实验绘制的图形,其中实验结果与图形对应准确的是( )
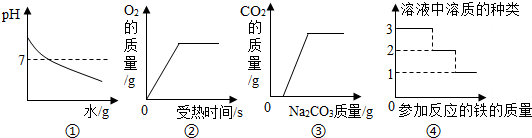

| A. | 图①是pH=13的NaOH溶液中加水稀释 | |
| B. | 图②是用适量的KClO3和MnO2混合物加热制O2 | |
| C. | 图③是向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量 | |
| D. | 图④向Cu(NO3)2和AgNO3的混合溶液中加入铁粉至过量 |
15.下列变化属于化学变化的是( )
| A. | 百炼成钢 | B. | 积水成渊 | C. | 铁杵成针 | D. | 滴水成冰 |

 化学反应中该原子比较容易得到(填“得到”或“失去”)电子变成S2-(填离子符号)
化学反应中该原子比较容易得到(填“得到”或“失去”)电子变成S2-(填离子符号)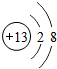 表示的是Al3+(填离子符号);
表示的是Al3+(填离子符号);