题目内容
10.为了除去粗盐中的CaCl2、MgCl2、Na2SO4及泥沙,可将粗盐溶于水,然后进行下列六步骤:①过滤,②加过量NaOH溶液,③加适量盐酸,④加过量Na2CO3溶液,⑤加过量BaCl2溶液,⑥蒸发,正确的操作顺序是②⑤④①③⑥(每项操作选用一次);①⑥均用到的仪器是玻璃棒;用物理方法除去粗盐中的可溶性杂质,可加入足量的饱和氯化钠溶液,再过滤.分析 根据镁离子用氢氧根离子沉淀,硫酸根离子用钡离子沉淀,钙离子用碳酸根离子沉淀,过滤要放在所有的沉淀操作之后,加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀,最后再用盐酸处理溶液中的碳酸根离子和氢氧根离子进行分析.
解答 解:镁离子用氢氧根离子沉淀,加入过量的氢氧化钠溶液可以将镁离子沉淀;硫酸根离子用钡离子沉淀,加入过量的氯化钡溶液可以将硫酸根离子沉淀;至于先除镁离子,还是先除硫酸根离子都可以;钙离子用碳酸根离子沉淀,除钙离子加入过量的碳酸钠溶液转化为沉淀,但是加入碳酸钠溶液要放在加入的氯化钡溶液之后,这样碳酸钠会除去反应剩余的氯化钡;完全反应后,进行过滤,再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,最后蒸发得到氯化钠,所以正确的顺序为:②⑤④①③⑥(合理即可).过滤和蒸发中均用到的仪器是玻璃棒;用物理方法除去粗盐中的可溶性杂质,可加入足量的饱和氯化钠溶液,再过滤.
故填:②⑤④①③⑥;玻璃棒;饱和氯化钠.
点评 本题难度较大,考查了粗盐提纯中离子的除杂,除去多种杂质离子时,要考虑除杂的顺序、后面加入的试剂要能除去前面加入的过量的试剂.

练习册系列答案
相关题目
20.类推是学习中常用的思维方法.现有一下类推结果,其中错误的是
①酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应;
②碱的水溶液显碱性,所以碱性溶液一定是碱溶液;
③氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物;
④复分解反应的反应物为两种化合物,生成物也是两种化合物,所以反应物为两种化合物,生成物也是两种化
合物的反应一定是复分解反应.( )
①酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应;
②碱的水溶液显碱性,所以碱性溶液一定是碱溶液;
③氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物;
④复分解反应的反应物为两种化合物,生成物也是两种化合物,所以反应物为两种化合物,生成物也是两种化
合物的反应一定是复分解反应.( )
| A. | 只有 ① | B. | 只有 ①②③ | C. | 只有②③④ | D. | ①②③④ |
18.下列物质中不作为空气污染物计入《环境空气质量标准》基本监测的是( )
| A. | 一氧化碳 | B. | 二氧化硫 | C. | 二氧化碳 | D. | PM10、PM2.5 |
5.下列各组物质在水溶液中能大量共存且无色的是( )
| A. | HCl NaNO3 K2SO4 Na2CO3 | B. | CuCl2 Na2SO4KNO3 NaCl | ||
| C. | NaOH K2CO3 NaCl Na2SO4 | D. | BaCl2 KNO3 CaC12 Na2SO4 |
19. 研究性学习小组的同学们在实验室中对某种家用制氧机制出的气体进行研究.
研究性学习小组的同学们在实验室中对某种家用制氧机制出的气体进行研究.
实验I:验证气体的性质.
把一小块燃着的木炭插入到盛有该气体的集气瓶中,观察到木炭燃烧更旺,反应的化学方程式为C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2.
实验II:测定气体中氧气的含量.
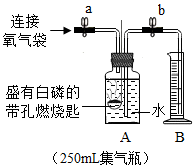
同学们在老师的指导下设计了如图所示装置,检查并确定装置的气密性良好,然后进行实验,并重复多次.(实验过程中由压强差引起的误差忽略不计)
[实验步骤]
①加入药品,将装置连接固定.
②打开止水夹a和b,向A中缓慢鼓入一定量气体后关闭止水夹a和b,观察到A中水进入到B中,B中水的体积为200mL.
③用凸透镜聚光引燃白磷,反应的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
④待白磷熄灭并冷却到室温,打开止水夹,观察到集气瓶中有剩余的气体的现象,说明收集的气体不是纯净的氧气.
⑤记录B中剩余水的体积.
[数据记录]
[数据处理和分析]
(1)在上表数据中,第1次数据偏差较大,导致产生较大误差的可能原因是实验时白磷不足.
(2)其余4组数据取平均值来进行计算,该家用制氧机制得的气体中氧气的体积分数约为80%.
 研究性学习小组的同学们在实验室中对某种家用制氧机制出的气体进行研究.
研究性学习小组的同学们在实验室中对某种家用制氧机制出的气体进行研究.实验I:验证气体的性质.
把一小块燃着的木炭插入到盛有该气体的集气瓶中,观察到木炭燃烧更旺,反应的化学方程式为C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2.
实验II:测定气体中氧气的含量.
同学们在老师的指导下设计了如图所示装置,检查并确定装置的气密性良好,然后进行实验,并重复多次.(实验过程中由压强差引起的误差忽略不计)
[实验步骤]
①加入药品,将装置连接固定.
②打开止水夹a和b,向A中缓慢鼓入一定量气体后关闭止水夹a和b,观察到A中水进入到B中,B中水的体积为200mL.
③用凸透镜聚光引燃白磷,反应的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
④待白磷熄灭并冷却到室温,打开止水夹,观察到集气瓶中有剩余的气体的现象,说明收集的气体不是纯净的氧气.
⑤记录B中剩余水的体积.
[数据记录]
| 实验次序 | 1 | 2 | 3 | 4 | 5 |
| B中剩余水体积/mL | 100 | 41 | 38 | 42 | 39 |
(1)在上表数据中,第1次数据偏差较大,导致产生较大误差的可能原因是实验时白磷不足.
(2)其余4组数据取平均值来进行计算,该家用制氧机制得的气体中氧气的体积分数约为80%.