题目内容
8.下列反应属于氧化还原反应的是( )| A. | CO2+Ca(OH)2→CaCO3↓+H2O | B. | S+O2 $\stackrel{点燃}{→}$ SO2 | ||
| C. | CuSO4+2NaOH→Cu(OH)2↓+Na2SO4 | D. | CaCO3 $\stackrel{焙烧}{→}$CaO+CO2↑ |
分析 氧化还原反应的实质为电子转移、特征为化合价升降,所以氧化还原反应中一定存在元素化合价变化,据此对各选项进行判断.
解答 解:A.CO2+Ca(OH)2→CaCO3↓+H2O,反应中不存在化合价变化,不属于氧化还原反应,故错误;
B.S+O2 $\stackrel{点燃}{→}$ SO2,中S、O元素的化合价发生变化,属于氧化还原反应,故B正确;
C.CuSO4+2NaOH→Cu(OH)2↓+Na2SO4,为复分解反应,反应中不存在化合价变化,不属于氧化还原反应,故错误;
D.CaCO3 $\stackrel{焙烧}{→}$CaO+CO2↑为分解反应,反应中不存在化合价变化,不属于氧化还原反应,故错误;
答案:B.
点评 本题考查了氧化还原反应的判断,题目难度不大,明确氧化还原反应的实质、特征为解答关键,注意掌握四种基本反应类型与氧化还原反应之间的关系,试题有利于提高学生的灵活应用能力.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
2.通过下列实验操作和现象能得出相应结论的是( )
| 实验操作 | 现象 | 结论 | |
| A | 向收集满CO2的软塑料瓶中加入约$\frac{1}{3}$体积的NaCl溶液,旋紧瓶盖,振荡 | 塑料瓶变瘪 | CO2能与NaCl反应 |
| B | 将未经打磨的Al条放入CuSO4溶液中 | 无明显现 | Al的活泼性低于Cu |
| C | 将白磷浸没在热水中,再向热水中的白磷通氧气 | 通氧气前白磷不燃烧,通氧气后白磷燃烧 | 氧气是燃烧需要的条件之一 |
| D | 点燃从导管放出的某气体,在火焰上方罩一个冷而干燥的烧杯 | 烧杯内壁有无色液滴产生 | 该气体是CH4 |
| A. | A | B. | B | C. | C | D. | D |
19.下列防锈措施不合理的是( )
| A. | 在自行车链条上涂油 | B. | 在车船的表面喷涂油漆 | ||
| C. | 在铁制水管表面镀锌 | D. | 擦去铝锅表面的氧化膜 |
16.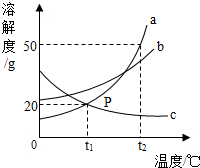 如图是a,b,c三种物质的溶解度曲线,下列分析不正确的是( )
如图是a,b,c三种物质的溶解度曲线,下列分析不正确的是( )
 如图是a,b,c三种物质的溶解度曲线,下列分析不正确的是( )
如图是a,b,c三种物质的溶解度曲线,下列分析不正确的是( )| A. | t2℃时,a,b,c三种物质的溶解度由大到小的顺序是a>b>c | |
| B. | t2℃时,将50g a物质放入100g水中充分溶解得到a的饱和溶液(a物质不含结晶水) | |
| C. | 将t2℃时 a,b,c三种物质的饱和溶液降温至t1℃时,所得溶液溶质质量分数关系是b>a>c | |
| D. | 将c的饱和溶液变为不饱和溶液,可采用升温的方法 |
3.以下四组离子,有一组能大量共存且能形成无色透明溶液,它应该是( )
| A. | Fe3+ SO42- H+ Cl- | B. | Mg2+ Cl- OH- Na+ | ||
| C. | H+ Ba2+ NO3- SO42- | D. | H+ Na+ K+ NO3- |
18.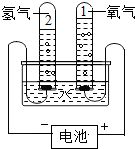 如图为电解水的实验,电解产物有氢气和氧气,反应方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,下列有关说法错误的是( )
如图为电解水的实验,电解产物有氢气和氧气,反应方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,下列有关说法错误的是( )
 如图为电解水的实验,电解产物有氢气和氧气,反应方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,下列有关说法错误的是( )
如图为电解水的实验,电解产物有氢气和氧气,反应方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,下列有关说法错误的是( )| A. | 氢气和氧气的体积比为2:1 | B. | 氢气和氧气的分子个数比为2:1 | ||
| C. | 氢气和氧气的质量比为2:1 | D. | 氢原子和氧原子的个数比为2:1 |
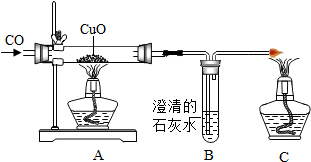 如图为CO还原CuO的实验装置图,请回答:
如图为CO还原CuO的实验装置图,请回答: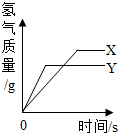 将等质量的锌粉和铁粉,分别放入相同质量分数的足量稀盐酸中,反应生成H2的质量与反应时间的关系如图所示,据图回答:
将等质量的锌粉和铁粉,分别放入相同质量分数的足量稀盐酸中,反应生成H2的质量与反应时间的关系如图所示,据图回答: