题目内容
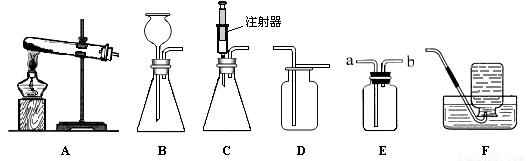
下图所示为实验室中常见的气体制备和收集装置。
请回答下列问题:
(1)实验室用高锰酸钾制取氧气,应选用发生装置 (填字母序号),反应的化学方程式为 。若用装置D收集氧气,验满的方法是 。
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,你认为选用C的优点是 。
(3)欲使用装置E用排空气法收集二氧化碳,则气体应从 (填“a”或“b”)端通入;欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从 (填“a”或“b”)端通入。
(4)已知一氧化氮气体难溶于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用图中
装置 (填字母序号)。
(5)在实验室里加热30g氯酸钾(KClO3)和二氧化锰的混合物制取氧气,完全反应后剩余固体质量为20.4g。请计算:
①生成氧气的质量为 g;
②原混合物中氯酸钾的质量。
(1)A 2KMnO4 △ K2MnO4 + MnO2+ O2↑ 将带火星的木条置于集气瓶口,木条复燃,证明已集满
(2)控制氧气产生的快慢和量的多少
(3)a b (4)F
(5)① 9.6g ②24.5g
【解析】
试题分析:(1)发生装置的选择依据:反应物的状态和反应条件,实验室用高锰酸钾制取氧气是加热固体高锰酸钾,故,应选用发生装置A,反应的化学方程式:2KMnO4 △ K2MnO4 + MnO2+ O2↑,若用装置D(向上排空气法)收集氧气,验满的方法:将带火星的木条置于集气瓶口,木条复燃,证明已集满
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,选用C的优点是:可以通过控制滴加液体的速率,从而控制控制氧气产生的快慢和量的多少
(3)欲使用装置E(万能瓶),用排空气法收集二氧化碳,由于二氧化碳的密度比空气大,故气体应从长管,即a端通入,欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体固定从短管进,即b端通入
(4)气体的收集装置的选择依据:气体的密度和溶解性,以及是否会与空气中的成分反应,由于一氧化氮气体难溶于水,在空气中容易与氧气发生反应,故只能用排水法收集,则收集一氧化氮气体时应选用图中装置F
(5)①根据质量守恒定律:化学反应前后,反应物各物质质量总和等于反应后生成的各物质质量总和 ,故生成氧气的质量=30g -20.4g= 9.6g
②根据化学反应方程式:2KClO3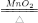 2KCl + 3O2 ↑中KClO3与O2的质量关系,即可求出氯酸钾的质量
2KCl + 3O2 ↑中KClO3与O2的质量关系,即可求出氯酸钾的质量
【解析】
设氯酸钾的质量为x
2KClO3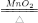 2KCl + 3O2 ↑
2KCl + 3O2 ↑
96
X 9.6g
245:96=x:9.6g
X=24.5g
答:氯酸钾的质量为24.5g
考点:发生、收集装置的选择依据,实验装置的优劣比较,质量守恒定律,根据化学方程式进行的计算

在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应的认识不正确的是
物质 | M | N | Q | P |
反应前质量(g) | 18 | 1 | 2 | 32 |
反应后质量(g) | X | 26 | 2 | 12 |
A.该变化的基本反应类型是分解反应 B.反应后物质M的质量为13g
C.反应中N、P的质量比为5︰4 D.物质Q可能是该反应的催化剂

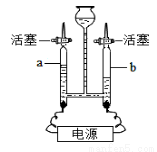
 2R+4K2O+3O2↑,则R是_______(填化学式)。
2R+4K2O+3O2↑,则R是_______(填化学式)。