题目内容
20. 在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究并回答问题.
在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究并回答问题.(1)【提出问题】假设l:红色粉末是铜粉;
假设2:红色粉末是氧化铁粉;
假设3:红色粉末是铜粉和氧化铁粉的混合物.
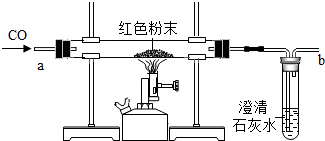
(2)【设计实验方案】同学们对实验作了如下设想和分析:取少量红色粉末放入硬质玻璃管中,通入一氧化碳片刻后加热至充分反应(实验装置如图所示).
请你完成下表:
| 实验中可能出现的现象 | 结论 |
| 假设1成立 | |
| 假设2成立 | |
| 假设3成立 |
(4)【反思与评价】
①实验过程中,硬质玻璃管内发生反应的化学方程式是3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
②实验时通入一氧化碳片刻后再加热的原因是防止加热一氧化碳和空气的混合气体时发生爆炸.
③从环保角度看,上面的实验装置有不足之处,请你对该装置进行改进,具体措施是在b处用酒精灯点燃,或用塑料袋(气球)收集.
分析 (1)根据题意,对红色粉末进行猜想;
(2)根据实验结论,分析支持结论应该出现的实验现象;
(4)对实验装置的操作进行解释及对存在问题进行改进.
解答 解:(1)该粉末是铜粉和氧化铁粉中的一种或两种,因此红色粉末可能为两物质的混合物;
(2)铜在高温下不与一氧化碳反应,因此粉末不变色,澄清石灰水也不会出现浑浊;氧化铁在高温下可与一氧化碳反应生成黑色铁粉和二氧化碳,充分反应后,粉末变黑色,澄清石灰水浑浊;
(4)①一氧化碳还原氧化铁生成铁和二氧化碳;化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
②一氧化碳具有可燃性,与空气混合点燃可能发生爆炸,因此应先通一氧化碳,待玻璃管内气体为纯净的一氧化碳时再进行加热,防止形成混合气体而引起爆炸;
③一氧化碳气体有毒,直接排放到空气中会造成空气污染,可把尾气进行燃烧或收集;故可在b处用酒精灯点燃,或用塑料袋(气球)收集;
故答案为:(1)铜粉和氧化铁粉的混合物;
(2)
| 红色粉末不变色,石灰水不变浑浊 | |
| 红色粉末全部变为黑色,石灰水变浑浊 | |
| 红色粉末部分变为黑色,石灰水变浑浊 |
点评 在作出猜想的时候要抓住题给的蛛丝马迹来进行猜想,不能盲目的乱猜,另外不纯的气体在点燃时有可能出现爆炸,所以在使用可燃性气体时,一定要注意检验气体的纯度.

练习册系列答案
相关题目
10.如图是气体分子的示意图,其中表示纯净物的是( )
| A. | 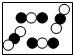 | B. | 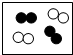 | C. |  | D. | 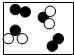 |
15. 鉴别碳酸钠溶液和氢氧化钠溶液的实验结束后,小红同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小红等几位同学对滤液的成分又进行了探究.
鉴别碳酸钠溶液和氢氧化钠溶液的实验结束后,小红同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小红等几位同学对滤液的成分又进行了探究.
(1)写出试管②中反应的化学方程式:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(2)【猜想】甲同学认为:只含氢氧化钠;
乙同学认为:只含碳酸钠;
丙同学认为:含有氢氧化钠和氢氧化钙;
丁同学认为:含有氢氧化钠、碳酸钠和氢氧化钙;
你认为还可能是含有氢氧化钠和碳酸钠(写一种猜想).
【讨论】你认为甲、乙、丙三位同学中那位同学的猜想不合理并叙述理由乙,滤液中一定含有氢氧化钠.
【实验设计】设计一个简单的实验证明你的猜想正确.
【实验分析】甲同学针对自己的猜想进行了如下实验:
你认为甲同学对实验结果判断是否正确?请说明理由不正确,如果含有氢氧化钠和氢氧化钙时,滴加适量的稀盐酸时无明显现象.
【反思拓展】
下列实验方法可以区分氢氧化钠和氢氧化钙两种固体的是ACD(填字母).
A.放置在空气中 B.观察颜色 C.加水溶解 D.利用溶解性.
 鉴别碳酸钠溶液和氢氧化钠溶液的实验结束后,小红同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小红等几位同学对滤液的成分又进行了探究.
鉴别碳酸钠溶液和氢氧化钠溶液的实验结束后,小红同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小红等几位同学对滤液的成分又进行了探究.(1)写出试管②中反应的化学方程式:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(2)【猜想】甲同学认为:只含氢氧化钠;
乙同学认为:只含碳酸钠;
丙同学认为:含有氢氧化钠和氢氧化钙;
丁同学认为:含有氢氧化钠、碳酸钠和氢氧化钙;
你认为还可能是含有氢氧化钠和碳酸钠(写一种猜想).
【讨论】你认为甲、乙、丙三位同学中那位同学的猜想不合理并叙述理由乙,滤液中一定含有氢氧化钠.
【实验设计】设计一个简单的实验证明你的猜想正确.
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,取滤液适量于试管中,滴加澄清石灰水 | 溶液变浑浊 | 你的猜想正确 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入少量稀盐酸 | 无明显现象 | 猜想成立 |
【反思拓展】
下列实验方法可以区分氢氧化钠和氢氧化钙两种固体的是ACD(填字母).
A.放置在空气中 B.观察颜色 C.加水溶解 D.利用溶解性.
5.下列方程式书写正确的是( )
| A. | 2KMnO4═K2MnO4+MnO2+O2↑ | B. | 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4↓ | ||
| C. | 2Na+H2SO4═Na2SO4+H2↑ | D. | H2O2$\frac{\underline{\;通电\;}}{\;}$H2↑+O2↑ |
12.下列选项中关于水的说法正确的是( )
| A. | 生活中采取蒸馏的方法将硬水软化 | |
| B. | 从电解水得到H2和O2,可知水是由氢原子和氧原子组成的 | |
| C. | 电解水得到的氢气和氧气质量比约为2:1 | |
| D. | 保持水的化学性质的最小粒子是水分子 |
10.下列关于物质组成的说法正确的是( )
| A. | 烧碱是混合物 | |
| B. | 煤气的主要成分是一氧化碳 | |
| C. | 乙醇中碳、氢、氧三种元素质量比为2:6:1 | |
| D. | 冰水是一种纯净物 |

 如图为硝酸钾和氯化钠两种物质的溶解度曲线示意图
如图为硝酸钾和氯化钠两种物质的溶解度曲线示意图