题目内容
6.推理是化学学习中常用的思维方法.下列推理正确的是( )| A. | 稀有气体原子的最外层电子数(He除外)是8,故最外层电子数为8的粒子一定是稀有气体原子 | |
| B. | 氧化物中含有氧元素,故含有氧元素的化合物一定是氧化物 | |
| C. | 置换反应有单质参加和生成,故置换反应中有元素化合价的改变. | |
| D. | 测定溶液的pH时,若用水将pH试纸湿润,测定结果一定不准确 |
分析 A、根据稀有气体的最外层电子数进行分析解答;
B、根据氧化物的概念解答;
C、根据置换反应的概念解答;
D、根据pH的测定方法解答.
解答 解:A、最外层电子数为8的粒子不一定是稀有气体原子,也可能是得失电子形成的阴阳离子,错误;
B、含有氧元素的化合物不一定是氧化物,例如氯酸钾含有三种元素不是氧化物,错误;
C、置换反应有单质参加和生成,故置换反应中有元素化合价的改变,正确;
D、测定溶液的pH时,若用水将pH试纸湿润,测定结果可能不准确,酸和碱的不准确,中性溶液不改变,错误;
故选C.
点评 本题考查的是对有关概念的理解,完成此题,可以依据已有的知识进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14. 硫酸是常见的酸,也是常用的化工原料.由于浓度不同,浓硫酸与稀硫酸在性质上存在较大差异,如浓硫酸具有脱水性、吸水性和强腐蚀性等.某课外兴趣小组为了探究浓硫酸的某些特性做了如下一些实验.请结合有关实验,按要求回答下列问题:
硫酸是常见的酸,也是常用的化工原料.由于浓度不同,浓硫酸与稀硫酸在性质上存在较大差异,如浓硫酸具有脱水性、吸水性和强腐蚀性等.某课外兴趣小组为了探究浓硫酸的某些特性做了如下一些实验.请结合有关实验,按要求回答下列问题:
(1)用玻璃棒蘸取少量浓硫酸在滤纸上写字,过后观察,字迹显黑色,这主要是由于浓硫酸具有脱水性,使纸中的纤维素炭化的缘故;在洗气瓶中盛放浓硫酸,除去氢气或氧气中的水分,是利用其吸水性.
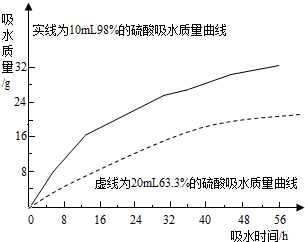
(2)探究浓硫酸的吸水性.兴趣小组把98%的硫酸10mL和63.3%的硫酸(用10mL98%的硫酸与10mL水配成)约20mL分别放入两个相同的大表面皿中,称量、观察、记录、分析.根据室温环境下实验的数据绘成的曲线如右图:
①稀释浓硫酸时,应将浓硫酸缓缓地注入盛有水的烧杯中并不断搅拌;
②由如图曲线你能得到的实验结论有哪些?(写两点)浓硫酸和一定浓度以上的稀硫酸都具有吸水性;浓硫酸吸水能力比稀硫酸强(吸水速度快、吸水量大)、开始两者吸水速度差异比较大,随着时间的推移吸水速度越来越接近,吸水能力越来越弱;硫酸浓度越稀吸水性越弱,到一定浓度后就失去吸水性;硫酸吸水能力可能会受环境温度、湿度、气压、酸的用量、表面积等因素的影响等.
(3)探究浓硫酸能否使铁钝化(钝化指在表面形成氧化膜保护层,使内层金属不再发生变化).可选用的实验药品有:相同铁片若干、浓硫酸、稀硫酸、硫酸铜溶液等.实验仪器任选.
①兴趣小组已经完成下表实验Ⅰ和Ⅱ,请你帮他们将实验报告补充完整.
你认为方案Ⅱ与方案Ⅰ相比,方案Ⅱ的优点是采用了对比实验的方法,更科学.
②某同学将一铁片插入盛有98%的浓硫酸的试管中,无明显变化,再给试管加热一段时间后,发现溶液变色并有刺激性气味气体产生,此现象说明:加热条件下,氧化膜被破坏(被浓硫酸溶解),铁继续与浓硫酸反应.(或热的浓硫酸能与铁反应产生刺激性气体;或热的浓硫酸不能使铁钝化;或铁的钝化随条件的改变而改变;或铁与浓硫酸的作用与温度有关)(其它合理答案均可).除产生该气体外,同时还生成硫酸铁和水,请写出反应的化学方程式:2Fe+6H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+6H2O+3SO2↑.
 硫酸是常见的酸,也是常用的化工原料.由于浓度不同,浓硫酸与稀硫酸在性质上存在较大差异,如浓硫酸具有脱水性、吸水性和强腐蚀性等.某课外兴趣小组为了探究浓硫酸的某些特性做了如下一些实验.请结合有关实验,按要求回答下列问题:
硫酸是常见的酸,也是常用的化工原料.由于浓度不同,浓硫酸与稀硫酸在性质上存在较大差异,如浓硫酸具有脱水性、吸水性和强腐蚀性等.某课外兴趣小组为了探究浓硫酸的某些特性做了如下一些实验.请结合有关实验,按要求回答下列问题:(1)用玻璃棒蘸取少量浓硫酸在滤纸上写字,过后观察,字迹显黑色,这主要是由于浓硫酸具有脱水性,使纸中的纤维素炭化的缘故;在洗气瓶中盛放浓硫酸,除去氢气或氧气中的水分,是利用其吸水性.
(2)探究浓硫酸的吸水性.兴趣小组把98%的硫酸10mL和63.3%的硫酸(用10mL98%的硫酸与10mL水配成)约20mL分别放入两个相同的大表面皿中,称量、观察、记录、分析.根据室温环境下实验的数据绘成的曲线如右图:
①稀释浓硫酸时,应将浓硫酸缓缓地注入盛有水的烧杯中并不断搅拌;
②由如图曲线你能得到的实验结论有哪些?(写两点)浓硫酸和一定浓度以上的稀硫酸都具有吸水性;浓硫酸吸水能力比稀硫酸强(吸水速度快、吸水量大)、开始两者吸水速度差异比较大,随着时间的推移吸水速度越来越接近,吸水能力越来越弱;硫酸浓度越稀吸水性越弱,到一定浓度后就失去吸水性;硫酸吸水能力可能会受环境温度、湿度、气压、酸的用量、表面积等因素的影响等.
(3)探究浓硫酸能否使铁钝化(钝化指在表面形成氧化膜保护层,使内层金属不再发生变化).可选用的实验药品有:相同铁片若干、浓硫酸、稀硫酸、硫酸铜溶液等.实验仪器任选.
①兴趣小组已经完成下表实验Ⅰ和Ⅱ,请你帮他们将实验报告补充完整.
| 方案 | 实验假设 | 实验方案 | 实验现象与结论 |
| Ⅰ | 能发生钝化 | 取一铁片先插入浓硫酸中,一段时间后取出,再插入硫酸铜溶液中. | 无明显变化,假设成立. |
| Ⅱ | 能发生钝化 | 取两片相同的铁片,一片放入浓硫酸中,一段时间后取出,与另一片同时放入硫酸铜溶液中. | 浸过浓硫酸的铁片表面无明显变化,另一铁片表面产生红色固体,假设成立. |
②某同学将一铁片插入盛有98%的浓硫酸的试管中,无明显变化,再给试管加热一段时间后,发现溶液变色并有刺激性气味气体产生,此现象说明:加热条件下,氧化膜被破坏(被浓硫酸溶解),铁继续与浓硫酸反应.(或热的浓硫酸能与铁反应产生刺激性气体;或热的浓硫酸不能使铁钝化;或铁的钝化随条件的改变而改变;或铁与浓硫酸的作用与温度有关)(其它合理答案均可).除产生该气体外,同时还生成硫酸铁和水,请写出反应的化学方程式:2Fe+6H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+6H2O+3SO2↑.
1.下列有关碳和碳的氧化物的说法正确的是( )
| A. | 金刚石、石墨和C60均为碳元素的有机物 | |
| B. | 除去CO2中的CO可用灼热的氧化铜 | |
| C. | 金刚石用作钻石,是因为金刚石硬度大 | |
| D. | 铅笔字迹易变模糊是因为常温下石墨的化学性质活泼 |
16.科学家最近研制成了以锶(Sr)原子做钟摆的“光格钟”,成了世界上取精确的钟.已知一种锶原子的相对原子质量为88,其质子数是38,下列说法正确的是( )
| A. | Sr可以表示一个锶元素 | B. | Sr2+ 核外有40个电子 | ||
| C. | SrCl2中含有氯分子 | D. | SrO属于金属氧化物 |

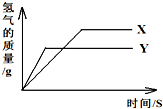 将等质量的锌粉和铁粉分别加入相同质量分数的足量稀盐酸中,反应生成氢气的质量与反应时间的关系如图所示,回答下列问题:
将等质量的锌粉和铁粉分别加入相同质量分数的足量稀盐酸中,反应生成氢气的质量与反应时间的关系如图所示,回答下列问题: