题目内容
4.下列实验操作、现象与结论对应关系正确的是( )| 选项 | 实验操作 | 现象 | 结论 |
| A | 向氢氧化钠固体中加入水 | 氢氧化钠固体消失 | 氢氧化钠与水发生了化学反应 |
| B | 用导管分别对准浸没在热水和冷水中的白磷通氧气 | 热水中的白磷燃烧, 冷水中的白磷不燃烧 | 燃烧条件之一是温度达到着火点 |
| C | 向溶质的质量分数为5%的过氧化氢溶液中加入少量氧化铜 | 有大量气泡产生 | 氧化铜起催化作用 |
| D | 向盐酸和氢氧化钙反应后的溶液中滴加酚酞 | 无明显现象 | 说明盐酸和氢氧化钙恰好反应 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据氢氧化钠固体易溶于水,进行分析判断.
B、燃烧需要同时满足三个条件:①可燃物、②氧气或空气、③温度要达到着火,接触进行分析判断.
C、向溶质的质量分数为5%的过氧化氢溶液中加入少量氧化铜,有大量气泡产生,氧化铜可能做催化剂,也可能是氧化铜与过氧化氢发生了化学反应.
D、酚酞溶液遇酸性溶液不变色,遇碱性溶液变红色.
解答 解:A、向氢氧化钠固体中加入水,氢氧化钠固体消失,可能是氢氧化钠溶于水造成的,不能证明氢氧化钠与水发生了化学反应,故选项实验操作、现象与结论对应关系错误.
B、用导管分别对准浸没在热水和冷水中的白磷通氧气,热水中的白磷燃烧,冷水中的白磷不燃烧,说明燃烧条件之一是温度达到着火点,故选项实验操作、现象与结论对应关系正确.
C、向溶质的质量分数为5%的过氧化氢溶液中加入少量氧化铜,有大量气泡产生,氧化铜可能做催化剂,也可能是氧化铜与过氧化氢发生了化学反应,不能氧化铜起催化作用,证明故选项实验操作、现象与结论对应关系错误.
D、向盐酸和氢氧化钙反应后的溶液中滴加酚酞,无明显现象,可能是盐酸和氢氧化钙恰好反应,也可能是盐酸过量,故选项实验操作、现象与结论对应关系错误.
故选:B.
点评 本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目
14.某无色溶液中大量存在的离子有H+、SO42-、Na+和另一种未知离子,该离子可能是( )
| A. | CO32- | B. | Fe2+ | C. | K+ | D. | OH- |
15.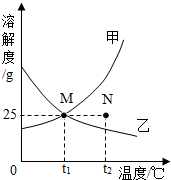 如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法错误的是( )
如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法错误的是( )
 如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法错误的是( )
如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法错误的是( )| A. | 甲物质的溶解度随温度的升高而增大 | |
| B. | 在t1℃时,甲、乙两物质的溶解度相等 | |
| C. | 在t2℃时,N点表示甲物质的不饱和溶液 | |
| D. | 在t1℃时,甲物质的饱和溶液中溶质的质量分数是25% |
19.如图所示装置中,容器Ⅰ、II体积相同,U形管内左右两侧液面相平,且装置气密性良好.实验时,打开分液漏斗旋塞,将液体同时滴入容器,滴加完毕后关闭旋塞.
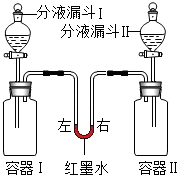
实验内容及相关现象如下表所示.
(1)实验A中,容器Ⅰ中的现象是石灰水变浑浊,容器Ⅱ中反应的化学方程式是H2O+CO2=H2CO3.
(2)实验B中,“①”的实验现象是右侧高左侧低,出现此现象的原因是等体积的氢氧化钠溶液比石灰水消耗的二氧化碳多.
(3)实验C中,依据盐酸浓度相同且足量,反应结束并恢复至室温后,红墨水液面位置计算出镁的质量为0.24g.

实验内容及相关现象如下表所示.
| 实验 编号 | 容器Ⅰ | 分液漏斗Ⅰ | 容器Ⅱ | 分液漏斗Ⅱ | 红墨水液面位置 |
| A | 二氧化碳 (充满) | 10mL澄清 石灰水 | 二氧化碳 (充满) | 10mL水 | 左侧高右侧低 |
| B | 二氧化碳 (充满) | 10mL澄清 石灰水 | 二氧化碳 (充满) | 10mL浓氢氧化钠溶液 | ① |
| C | 0.65g锌 | 10mL盐酸 | 镁 | 10mL盐酸 | 室温时恢复至起始状态 |
(2)实验B中,“①”的实验现象是右侧高左侧低,出现此现象的原因是等体积的氢氧化钠溶液比石灰水消耗的二氧化碳多.
(3)实验C中,依据盐酸浓度相同且足量,反应结束并恢复至室温后,红墨水液面位置计算出镁的质量为0.24g.
13.物质的性质决定用途,用途反映性质.请填写下面表格.
| 物质 | 性质 | 用途 |
| 干冰 | 升华吸热 | ①做制冷剂 |
| 生石灰 | ②与水反应生成氢氧化钙 | 用作干燥剂 |
 化学小组同学设计了如图所示实验方案.
化学小组同学设计了如图所示实验方案.