题目内容
15. 阅读材料,回答问题:
阅读材料,回答问题:材料1:镁(Mg)为银白色金属:熔点648.8℃,沸点11.7℃,密度1.74克/厘米3.镁具有优良的切削加工性能.
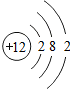
材料2:镁原子的结构示意图如图,在化学反应中易失去2个电子,达到8电子的稳定结构,单质镁的化学性质很活泼,在空气中被直接氧化,且镁在空气中燃烧时发出耀眼光焰,所以用来制作照明弹、燃烧弹和焰火等.
材料3:燃烧不一定要有氧气参加,任何发光、发热的剧烈的化学反应,都可以叫做燃烧,镁带在点燃的条件下,可以在二氧化碳由燃烧生成氧化镁和碳.
(1)镁离子最外层电子数为8.
(2)请写出一点有关镁的性质:①物理性质银白色金属,熔点648.8℃,沸点11.7℃,密度1.74克/厘米3;②化学性质能与氧气和二氧化碳反应.
(3)镁是一种活泼金属,根据所学化学知识你认为保存镁条时应当:密封.
(4)写出材料2中的化学方程式2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
(5)写出材料3中的化学方程式2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
分析 根据离子的形成进行分析解答,物理性质是指不需要发生化学变化就表现出来的性质;化学性质则需要发生化学变化表现出来;根据性质确定保存方法;根据反应物和生成物以及反应的条件书写反应的化学方程式.
解答 解:(1)镁原子失去最外层的两个电子变为镁离子,镁离子最外层电子数为8,故填:8.
(2)①镁是一种银白色金属,熔点648.8℃,沸点11.7℃,密度1.74克/厘米3,属于镁的物理性质,故填:银白色金属,熔点648.8℃,沸点11.7℃,密度1.74克/厘米3;
②根据题干提供的信息可以看出,镁能在空气中和二氧化碳中燃烧,这属于镁的化学性质,故填:能与氧气和二氧化碳反应;
(3)镁是一种活泼金属,保存镁条时应当密封,故填:密封;
(4)写出材料2中镁和氧气反应生成氧化镁,故填:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;
(5)写出材料3中镁和二氧化碳反应生成氧化镁和碳,故填:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
点评 本题考查的是金属镁性质的实验探究以及化学方程式的书写的知识,完成此题,可以依据题干提供的信息结合已有的知识进行.

练习册系列答案
 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
6.小丽同学用连线的方式对某一主题知识进行如下归纳,其中有错误的一组( )
| A. | 性质与用途 天然最硬的物质--镶玻璃刀头 防菜刀生锈--刷油漆 | |
| B. | 生活常识 熟石灰呈碱性--改良酸性士壤 取暖防中毒--煤炉上放一壶水 | |
| C. | 元素与人体健康 人体缺碘--甲状腺肿大 减少白色污染--使用可降解塑料 | |
| D. | 环保与物质的利用 人体缺氟--易生龋 减少水质污染--禁止生产含磷洗衣粉 |
10.下列物质变化中只发生物理变化的是( )
| A. | 湖水蒸发 | B. | 瓦斯爆炸 | C. | 燃放烟花 | D. | 铁锤生锈 |
20.下列现象的微观解释中,不正确的是( )
| A. | 氢气与液氢都可做燃料一一相同物质的分子,其化学性质相同 | |
| B. | 用警犬搜救地震中被埋人员一一分子在不断运动 | |
| C. | 用水银体温计测量体温一一温度升高,原子间间隔增大 | |
| D. | l体积酒精和1体积水混合后小于2体积一一分子变小了 |
4.下列实验现象描述正确的是( )
| A. | 红磷燃烧,产生大量白烟 | |
| B. | 蜡烛燃烧,生成二氧化碳和水 | |
| C. | 10mL水和10mL酒精混合后凹液面最近处在量筒20mL刻度处 | |
| D. | 电解水实验中,正极的气体能燃烧 |