题目内容
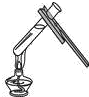
【题目】根据如图甲实验装置图,回答有关问题,
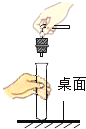
(1)装置图中仪器a的名称为 .
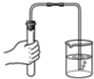
(2)用氯酸钾和二氧化锰混合共热制取氧气,可选用的装置组合是 , 写出发生反应的化学方程式 . 若改用高锰酸钾制取氧气,发生装置应作的改动是 .
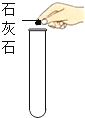
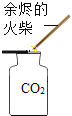
(3)实验室利用B装置制取二氧化碳的化学方程式为 , 如果利用G装置收集二氧化碳,气体应从 端通入(填“b”或“c”),用C装置代替B装置作为发生装置,其主要优点是 .
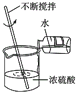
(4)某学生想要通过碳酸氢铵分解产生的氨气来探究氨水具有碱性,而氨气不具有碱性,按如图乙所示进行实验:(滤纸条用酚酞试液浸泡并晾干)
[资料] NH4HCO3![]() NH3↑+H2O+CO2↑ 2NH3+H2SO4═(NH4)2 SO4
NH3↑+H2O+CO2↑ 2NH3+H2SO4═(NH4)2 SO4
试分析:A装置中加入浓硫酸的作用是 , B中氢氧化钠固体的作用是:Ⅰ.干燥气体;Ⅱ.(用化学方程式表示),该同学看到现象,得出了正确的结论.
【答案】
(1)集气瓶
(2)AD或AF;2KClO3![]() 2KCl+3O2↑;在试管口放一小团棉花
2KCl+3O2↑;在试管口放一小团棉花
(3)CaCO3+2HCl=CaCl2+CO2↑+H2O;b;随时控制反应的开始与停止,控制反应速率
(4)浓硫酸溶于水放热,提供热量;CO2+2NaOH=Na2CO3+H2O;干燥的滤纸条不变红,湿润的滤纸条变红
【解析】解:(1)仪器a是集气瓶,故填:集气瓶;(2)实验室用氯酸钾和二氧化锰混合制取氧气,属于固体加热型,故应选用的发生装置是A,反应方程式是:2KClO3![]() 2KCl+3O2↑,氧气的密度比空气大,不易溶于水,可用排水法或向上排空气法来收集;高锰酸钾制取氧气应在试管口放一团棉花,防止加热时高锰酸钾粉末进入导管;故填:AD或AF;2KClO3
2KCl+3O2↑,氧气的密度比空气大,不易溶于水,可用排水法或向上排空气法来收集;高锰酸钾制取氧气应在试管口放一团棉花,防止加热时高锰酸钾粉末进入导管;故填:AD或AF;2KClO3![]() 2KCl+3O2↑;在试管口放一小团棉花;(3)二氧化碳的实验室制法是用稀盐酸与大理石(或石灰石.其主要成分都是碳酸钙)反应来制取.其反应原理是CaCO3+2HCl=CaCl2+CO2↑+H2O;因二氧化碳的密度比空气大,如用G装置收集CO2 , 则气体应从b端入;用C装置代替B装置作为发生装置,能随时控制反应的开始与停止,控制反应速率;故填:CaCO3+2HCl=CaCl2+CO2↑+H2O;b;随时控制反应的开始与停止,控制反应速率;(4)浓硫酸溶于水放热,因此向A烧杯中加浓硫酸的作用是放热使NH4HCO3分解;氢氧化钠固体既吸收水蒸气,又吸收二氧化碳;干燥的氨气不具有碱性,石蕊试纸不变色;氨气溶于水生成氨水,D瓶中石蕊试纸变蓝色;故填:浓硫酸溶于水放热,提供热量;
2KCl+3O2↑;在试管口放一小团棉花;(3)二氧化碳的实验室制法是用稀盐酸与大理石(或石灰石.其主要成分都是碳酸钙)反应来制取.其反应原理是CaCO3+2HCl=CaCl2+CO2↑+H2O;因二氧化碳的密度比空气大,如用G装置收集CO2 , 则气体应从b端入;用C装置代替B装置作为发生装置,能随时控制反应的开始与停止,控制反应速率;故填:CaCO3+2HCl=CaCl2+CO2↑+H2O;b;随时控制反应的开始与停止,控制反应速率;(4)浓硫酸溶于水放热,因此向A烧杯中加浓硫酸的作用是放热使NH4HCO3分解;氢氧化钠固体既吸收水蒸气,又吸收二氧化碳;干燥的氨气不具有碱性,石蕊试纸不变色;氨气溶于水生成氨水,D瓶中石蕊试纸变蓝色;故填:浓硫酸溶于水放热,提供热量;
CO2+2NaOH=Na2CO3+H2O;干燥的滤纸条不变红,湿润的滤纸条变红.
【考点精析】解答此题的关键在于理解制取氧气的操作步骤和注意点的相关知识,掌握制取氧气的操作步骤(以高锰酸钾制取氧气并用排水法收集为例)a、步骤:查—装—定—点—收—移—熄,以及对书写化学方程式、文字表达式、电离方程式的理解,了解注意:a、配平 b、条件 c、箭号.

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案【题目】科学兴趣小组的同学在老师的指导下,对用铁碳合金制作的井盖中单质铁的含量进行了测定.他们请老师将一块破碎的井盖样品进行粉碎处理,四组同学各取12.0g 粉末样品罝于烧杯中,然后加入一定质量的稀硫酸,充分反应后,对烧杯中剩余固体进行称量,相关的实验数据记录如表:
组别 | 样品质量/g | 加入稀硫酸质量/g | 剩余固体 |
1 | 12.0 | 80.0 | 0.8 |
2 | 12.0 | 80.0 | 0.8 |
3 | 12.0 | 100.0 | 1.0 |
4 | 12.0 | 100.0 | 0.8 |
(1)分析上表数据可知,编号为组的同学其剩余固体质量的数据不合理.
(2)该井盖样品中单质铁的质量分数=(结果保留至0.1%)
(3)反应所用硫酸溶液中溶质的质量分数是多少?(写出计算过程)
(4)如果井盖已生锈,你认为要准确地测得样品中铁元素的质量分数,应该将上述实验中测量“剩余固体质量”改成测量下列中的(填字母).
A.加入稀硫酸的体积
B.反应完全后烧杯中所有物质的质量
C.反应完全后烧杯中所有物质的质量和剩余固体质量.
【题目】一些物质在常温下的近似pH如下表:
物质 | 血浆 | 胃液 | 正常雨水 | 葡萄汁 |
pH | 7.35~7.45 | 0.9~1.5 | ≈5.6 | 3.5~4.5 |
下列有关上述四种物质的说法中正确的是( )
A.只有葡萄汁显酸性
B.只有血浆显碱性
C.正常雨水显中性
D.胃酸过多的人应多饮用葡萄汁