题目内容
12. 在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究.
在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究.【查阅资料】(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成.
(2)氯化钙、氯化钡溶液均呈中性.
【提出问题】(1)酒精中是否含有碳元素?(2)固体酒精中的氢氧化钠是否变质?
【实验探究】
(1)按如图实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论.
此结论合理(选填“合理”或“不合理”)
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀.取沉淀于试管中加稀盐酸,有气泡产生.分析实验并结合资料得出氢氧化钠已变质.写出氢氧化钠变质或碳酸钠反应的化学方程式2NaOH+CO2═Na2CO3+H2O或CaCO3+2HCl=CaCl2+CO2↑+H2O.
(3)为进一步确定氢氧化钠的变质程度,分组探究.
①甲组取烧杯上层清液于两支试管中,按下图探究.
| 方案 | 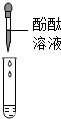 |  |
| 现象 | 溶液变红 | 产生 |
| 结论 | 清液中有氢氧化钠 | 清液中有碳酸钙 |
【实验结论】:经过讨论一致认为固体酒精中氢氧化钠部分(填“全部”或“部分”)变质.
【反思交流】:乙组实验中加足量氯化钡溶液的目的是除去碳酸钠,防止影响对NaOH的检验.
分析 【实验探究】
(1)酒精燃烧生成水和二氧化碳,二氧化碳能使澄清石灰水变浑浊;
(2)氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水,碳酸钠能和氯化钙反应生成碳酸钙沉淀和氯化钠,碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳;
(3)氢氧化钠溶液和碳酸钠溶液都显碱性,都能够使酚酞试液变红色;
【实验结论】由实验现象分析;
【反思交流】为了使碳酸钠完全反应,应该加入过量的氯化钡溶液.
解答 解:【实验探究】
(1)由质量守恒定律,发现澄清石灰水变浑浊,说明反应生成了二氧化碳,因为酒精燃烧时只有氧气参加,因此可得出酒精中含有碳元素的结论,此结论合理.
故填:合理.
(2)氢氧化钠易吸收空气中的水而潮解,吸收空气中的二氧化碳生成碳酸钠而变质,氢氧化钠变质的化学方程式:2NaOH+CO2═Na2CO3+H2O;
白色沉淀是碳酸钠和氯化钙反应生成的碳酸钙,碳酸钙和稀盐酸反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O.
故填:2NaOH+CO2═Na2CO3+H2O或CaCO3+2HCl=CaCl2+CO2↑+H2O.
(3)①取烧杯上层清夜于两支试管中,其中一只试管中产生白色沉淀,说明清液中有碳酸钠.
故填:白色沉淀.
②乙组认为甲组实验不能证明清夜中一定有氢氧化钠,理由是:碳酸钠溶液显碱性,也能使酚酞试液变红色.
故填:碳酸钠溶液呈碱性;也能使酚酞溶液变红.
【实验结论】由实验现象可知滤液中含有氢氧化钠和碳酸钠,氢氧化钠部分变质
【反思交流】
乙组实验中加足量氯化钡溶液的目的是除去碳酸钠,防止影响对NaOH的检验.
故填:除去碳酸钠,防止影响对NaOH的检验.
点评 实验是化学的重要组成部分,正确的实验操作是得出科学结论的前提条件之一,因此要学会设计实验、进行实验、分析实验,为得出正确的结论奠定基础.

| A. | 铁丝和硫酸铜溶液反应:银白色固体表面产生紫红色固体 | |
| B. | 碳酸钠溶液与氢氧化钙溶液反应:溶液中产生气泡 | |
| C. | 氢气在空气中燃烧:无色气体燃烧,发出淡蓝色火焰,放热 | |
| D. | 镁条在空气)中燃烧:银白色固体燃,生成白色固体氧化镁 |
| A. | 几天后,三份固体的质量由小到大的顺序为:A=B=C | |
| B. | 为控制正好反应,A可用酚酞试液指示,B、C可滴加稀硫酸直到正好不冒气泡 | |
| C. | 正好反应时,消耗稀硫酸的质量由大到小的顺序为:A>B>C | |
| D. | 正好反应时,生成硫酸钠的质量都相等,均为35.5g |
| A. | 该反应是复分解反应 | |
| B. | 氯化铵作为化肥不能与氢氧化钙混合施用 | |
| C. | 反应前后钙元素的质量不变 | |
| D. | 制得的氨气可以用向上派空气法收集 |
| A. | FeCl3、CuSO4、NaCl | B. | BaCI2、Na2SO4、NaOH | ||
| C. | CaCl2、Na2CO3、AgNO3 | D. | K2SO4、NaNO3、HCl |
| A. | 完全反应得到无色溶液,样品中一定没有铁 | |
| B. | 反应后过滤,一定会有滤渣 | |
| C. | 所加稀盐酸中溶质的质量分数为7.3% | |
| D. | 反应后过滤,得到溶液中溶质只有氯化镁 |
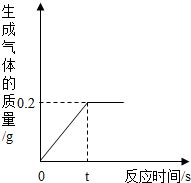 李晔同学取10g粗锌样品(所含杂质不溶于水,也不与酸反应)于烧杯中,向其中加入143.7g稀硫酸时,恰好完全反应.生成气体的质量与反应时间的关系如图所示,请计算:
李晔同学取10g粗锌样品(所含杂质不溶于水,也不与酸反应)于烧杯中,向其中加入143.7g稀硫酸时,恰好完全反应.生成气体的质量与反应时间的关系如图所示,请计算: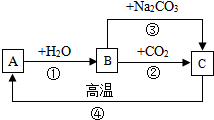 A、B、C是三种常见的含钙化合物.它们之间有如图所示的转化关系(部分产物略去).
A、B、C是三种常见的含钙化合物.它们之间有如图所示的转化关系(部分产物略去).