题目内容
9.N(NO2)3是科学家2011年发现的一种新型火箭燃料.下列有关说法正确的是( )| A. | N(NO2)3中氮元素和氧元素的原子个数是2:5 | |
| B. | N(NO2)3中氮元素和氧元素的质量比是7:4 | |
| C. | N(NO2)3相对分子质量是152g | |
| D. | N(NO2)3氮元素的质量分数是36.8% |
分析 A.根据化学式的意义来分析;
B.根据化合物中元素质量比的计算方法来分析;
C.根据相对分子质量的单位来分析;
D.根据化合物中元素质量分数的计算方法来分析.
解答 解:A.一个N(NO2)3分子由4个氮原子和6个氧原子构成的,故氮原子与氧原子的个数比为:4:6=2:3,故错误;
B.N(NO2)3中N、O两元素的质量比是(14×4):(16×6)=7:12,故错误;
C.相对分子质量的单位不是“g”而是“1”,通常省略不写,故错误;
D.N(NO2)3中N元素的质量分数为$\frac{14×4}{14+(14+16×2)×3}×100%$≈36.8%,故正确.
故选:D.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
4.二氧化硫、氧气、氧化铜含有相同的( )
| A. | 氧气 | B. | 氧元素 | C. | 氧分子 | D. | 两种元素 |
1.鉴别氧气、空气、二氧化碳、一氧化碳四种气体最简便方法是( )
| A. | 观察气体颜色 | B. | 观察它们各自在水中溶解性 | ||
| C. | 用燃着木条分别伸入瓶中 | D. | 用紫色石蕊试液检验 |
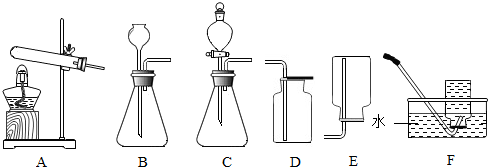
 如图所示是实验室制取氢气的一种简易装置图,根据装置回答问题:
如图所示是实验室制取氢气的一种简易装置图,根据装置回答问题: