题目内容
4.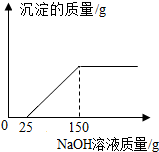 现有16g Fe2O3和CuO的混合物,进行如下实验;把混合物全部加入到100克足量的硫酸溶液中,完全溶解后,滴加溶质质量分数为16%的氢氧化钠溶液,滴加氢氧化钠溶液的质量与生成沉淀质量的关系如图所示,回答下列问题:
现有16g Fe2O3和CuO的混合物,进行如下实验;把混合物全部加入到100克足量的硫酸溶液中,完全溶解后,滴加溶质质量分数为16%的氢氧化钠溶液,滴加氢氧化钠溶液的质量与生成沉淀质量的关系如图所示,回答下列问题:(1)写出上述实验过程中会生成红褐色沉淀的化学方程式:6NaOH+Fe2(SO4)3=2Fe(OH)3↓+3Na2SO4.
(2)当所加氢氧化钠溶液质量为20g时,混合液中的溶质有Fe2(SO4)3、H2SO4、CuSO4、Na2SO4.
(3)求CuO的质量.
分析 (1)氧化铁与硫酸反应生成硫酸铁和水,硫酸铁与氢氧化钠反应生成氢氧化铁和硫酸钠;
(2)氧化铁与硫酸反应生成硫酸铁和水,氧化铜与硫酸反应生成硫酸铜和水,由于加入足量的硫酸溶液,再滴加氢氧化钠溶液时,氢氧化钠优先于硫酸反应;
(3)根据电荷守恒知道,铁和铜所带正电荷总数必与氢氧根离子所带负电荷总数相等.
解答 解:(1)氧化铁与硫酸反应生成硫酸铁和水,硫酸铁与氢氧化钠反应生成氢氧化铁和硫酸钠,方程式为:6NaOH+Fe2(SO4)3=2Fe(OH )3↓+3Na2SO4;
(2)氧化铁与硫酸反应生成硫酸铁和水,氧化铜与硫酸反应生成硫酸铜和水,由于加入足量的硫酸溶液,再滴加氢氧化钠溶液时,氢氧化钠优先于硫酸反应,当所加氢氧化钠溶液质量为20g时,氢氧化钠还没有把硫酸消耗完,所以混合液中的溶质有Fe2(SO4)3、H2SO4、CuSO4、Na2SO4;
(3)设Fe2O3的质量为x,CuO的质量为y.
则有x+y=16g--①
根据电荷守恒知道,铁和铜所带正电荷总数必与氢氧根离子所带负电荷总数相等.可得方程
$\frac{x}{160}$×2×3+$\frac{y}{80}$×1×2=$\frac{(150g-25g)×16%}{40}$--②
有①②解得x=y=8g
故答案为:(1)6NaOH+Fe2(SO4)3=2Fe(OH )3↓+3Na2SO4;
(2)Fe2(SO4)3、H2SO4、CuSO4、Na2SO4;
(3)8g.
点评 此题是数形结合类问题,分析反应的关系图是正确判断反应进行的依据和基础.弄清折点的含义,是解决此题的关键之所在.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.下列药品与水接触后,温度降低的是( )
| A. | 烧碱 | B. | 硝酸铵 | C. | 浓硫酸 | D. | 氯化钠 |
19.常温下,饱和石灰水的pH约为11.3,现往一定量饱和石灰水中加入下列固体物质,恢复到常温时,溶液的pH一定不会发生改变的是( )
| A. | NaOH | B. | MgCl2 | C. | Na2CO3 | D. | CaO |
9. 质量相等的两种金属a和b,它们都能与稀硫酸发生反应并产生氢气,反应情况如图所示,则下列有关a、b的活动性和参加反应的稀硫酸的质量的说法中,正确的是( )
质量相等的两种金属a和b,它们都能与稀硫酸发生反应并产生氢气,反应情况如图所示,则下列有关a、b的活动性和参加反应的稀硫酸的质量的说法中,正确的是( )
①a比b活泼 ②b比a活泼 ③酸不足 ④酸过量.
 质量相等的两种金属a和b,它们都能与稀硫酸发生反应并产生氢气,反应情况如图所示,则下列有关a、b的活动性和参加反应的稀硫酸的质量的说法中,正确的是( )
质量相等的两种金属a和b,它们都能与稀硫酸发生反应并产生氢气,反应情况如图所示,则下列有关a、b的活动性和参加反应的稀硫酸的质量的说法中,正确的是( )①a比b活泼 ②b比a活泼 ③酸不足 ④酸过量.
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
13.据2015年央视315晚会曝光,山东省东营市、滨州市许多不法厂商生产不合格的“调和汽油”,生产的93号汽油是把一部分90号的汽油配上大量的石脑油、芳烃和MTBE(抗暴剂)等各种化工原料简单混合而成.这种汽油损害汽车,污染环境,影响健康.MTBE的化学式为CH3OC(CH3)3. 以下关于MTBE的说法中,不正确的是( )
| A. | “MTBE”是一种有机物 | |
| B. | 一个“MTBE”分子由18个原子构成 | |
| C. | “MTBE”分子中,碳、氢、氧的质量比为5:12:1 | |
| D. | “MTBE”完全燃烧后,生成水和二氧化碳的质量比为55:27 |
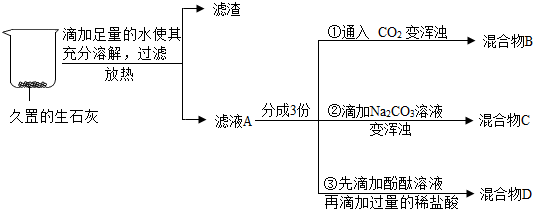
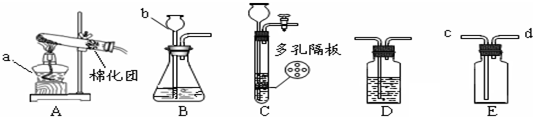
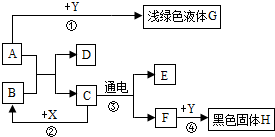 如图所示,A~H是初中化学常见的物质,A和B可发生中和反应,C为生活中最常见的液体,F可供给呼吸,X常用作食品干燥剂,Y为单质,请根据图示回答下列问题:
如图所示,A~H是初中化学常见的物质,A和B可发生中和反应,C为生活中最常见的液体,F可供给呼吸,X常用作食品干燥剂,Y为单质,请根据图示回答下列问题: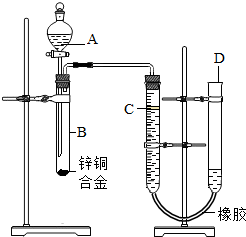 某学习小组用如图所示装置测定锌铜合金中铜的质量分数.(已知:金属与酸时放出一定的热量)
某学习小组用如图所示装置测定锌铜合金中铜的质量分数.(已知:金属与酸时放出一定的热量)