题目内容
3.根据如图实验,回答有关问题: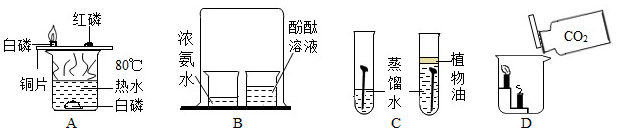
(1)A实验中热水的作用提供热量和使烧杯中的白磷隔绝氧气;
(2)B实验的目的是证明分子在不断的运动;
(3)C实验中甲试管的铁钉生锈乙试管的铁钉不生锈,说明铁生锈与水和氧气有关.
(4)根据D实验得到的结论,推测二氧化碳的用途之一是灭火.
分析 根据热水能提供热量和使烧杯中的白磷隔绝氧气的作用解答;根据氨水具有挥发性解答;根据铁生锈的条件进行分析解答;根据二氧化碳的性质解答.
解答 解:(1)A实验中的热水能给铜片上的白磷和红磷提供热量,同时能使烧杯中的白磷隔绝氧气,故填:提供热量和使烧杯中的白磷隔绝氧气;
(2)氨水能挥发出氨气,运动到酚酞试液中使酚酞变红,想证明分子在不断的运动,故填:证明分子在不断的运动;
(3)C实验中乙试管中的铁钉不与水和氧气接触,而甲中的铁钉与水和氧气接触,说明铁生锈需要与水和氧气接触,故填:水和氧气;
(3)向烧杯中的阶梯蜡烛倾倒二氧化碳,下层的蜡烛先熄灭,上层的蜡烛后熄灭,说明二氧化碳既不能燃烧也不能支持燃烧且密度大于空气,故可以用于灭火,故填:灭火.
(3)撤去酒精灯时,试管内温度降低,石灰水能够倒吸进入试管中;铜在高温条件下能够被空气中的氧气氧化成氧化
点评 本题主要考查燃烧的条件、金属锈蚀的条件的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案
相关题目
11.据中央电视台1991年6月3日对云南抚仙湖湖底古城考古的现场报道,科学家曾通过测定古生物遗骸中的碳-14含量来推断古城年代,碳-14原子的核电荷数为6,相对原子质量为14.下列关于碳-14原子的说法中,错误的是( )
| A. | 中子数为6 | B. | 质子数为6 | ||
| C. | 电子数为6 | D. | 质子数和中子数之和是14 |
18.规范的实验操作是实验成功的保证,下列实验操作正确的是( )
| A. |  点燃酒精 | B. | 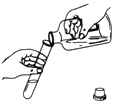 取用液体 | C. | 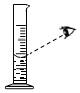 读取体积 | D. | 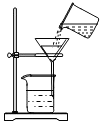 过滤 |
15.下表中,除去物质所含杂质的方法正确的是( )
| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | NaCl溶液 | Na2CO3 | 加入稀盐酸至不再产生气泡 |
| B | CuO粉末 | C | 加入过量稀盐酸,充分反应 |
| C | MnO2 | KCl | 溶解、过滤、蒸发结晶 |
| D | KCl溶液 | CuCl2 | 加入氢氧化钠溶液至不再产生沉淀 |
| A. | A | B. | B | C. | C | D. | D |
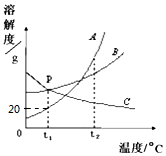 根据如图A、B、C三种固体的溶解度曲线回答:(A、B、C析出晶体时均不含结晶水)
根据如图A、B、C三种固体的溶解度曲线回答:(A、B、C析出晶体时均不含结晶水)