题目内容
15.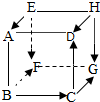 如图表示几种常见物质之间的转化关系,实现或虚线相连的两种物质之间能够发生反应,箭头表示一种物质能向另一种物质转化.已知A、C为黑色粉末,B为单质,A与D的反应早在西汉时期书籍中就有记载:“曾青得铁则化为铜”,F与G的反应时大自然应用太阳能最成功的范例,A、B、G三种物质可发生反应,生成物的主要成分是红棕色的E.请完成下列内容:
如图表示几种常见物质之间的转化关系,实现或虚线相连的两种物质之间能够发生反应,箭头表示一种物质能向另一种物质转化.已知A、C为黑色粉末,B为单质,A与D的反应早在西汉时期书籍中就有记载:“曾青得铁则化为铜”,F与G的反应时大自然应用太阳能最成功的范例,A、B、G三种物质可发生反应,生成物的主要成分是红棕色的E.请完成下列内容:(1)B的化学式为O2;G的化学式为H2O;F的用途灭火(写一点).
(2)“曾青得铁则化为铜”表示的化学方程式Fe+CuSO4═FeSO4+Cu;H与C反应的化学方程式CuO+H2SO4═CuSO4+H2O.
(3)上述物质中没有出现的物质类别是碱(选填:单质、氧化物、酸、碱、盐).
分析 根据题干提供的信息结合已有的物质的性质进行分析解答,A是黑色粉末,A与D的反应早在西汉时期我国书籍中就有记载,故该反应是铁与硫酸铜的反应,故A是铁,D是硫酸铜;F与G的反应是大自然应用太阳能最成功的范例,则该反应是光合作用,F和G是二氧化碳和水,C是黑色粉末,能生成G,能生成硫酸铜,故C是氧化铜,氧化铜被一氧化碳还原生成铜和二氧化碳,故G是水,F是二氧化碳;铁能与B反应,B能生成氧化铜,故B是氧气;H能生成硫酸铜,能生成二氧化碳,故H可能是硫酸;E能生成铁,能生成水,其能与硫酸反应,故E可能是氧化铁,据此解答.
解答 解:根据A是黑色粉末,A与D的反应早在西汉时期我国书籍中就有记载,故该反应是铁与硫酸铜的反应,故A是铁,D是硫酸铜;F与G的反应是大自然应用太阳能最成功的范例,则该反应是光合作用,F和G是二氧化碳和水,C是黑色粉末,能生成G,能生成硫酸铜,故C是氧化铜,氧化铜被一氧化碳还原生成铜和二氧化碳,故;铁能与B反应,B能生成氧化铜,故B是氧气;H能生成硫酸铜,能生成二氧化碳,故H可能是硫酸;E能生成铁,能生成水,其能与硫酸反应,故E可能是氧化铁,带入框图,推断合理;
(1)根据分析,B是氧气,G是水,F是二氧化碳,故B的化学式为O2;G的化学式为H2O;F的用途灭火;
(2)曾青得铁则化为铜中的曾青是说的铜的化合物,即用铁将铜的化合物中的铜元素置换出来,反应物是铁和硫酸铜,生成物是硫酸亚铁和铜,不需要反应条件,所以化学方程式是:Fe+CuSO4═FeSO4+Cu;
根据分析,H是硫酸,C是氧化铜,H与C反应,即硫酸和氧化铜反应的化学反应方程式为:CuO+H2SO4═CuSO4+H2O;
(3)根据分析,A是铁,属于单质,B是氧气,属于单质,C是氧化铜,属于氧化物,D是硫酸铜,属于盐,E是氧化铁,属于氧化物,F是二氧化碳,属于氧化物,G是水,属于氧化物,H是硫酸,属于酸,没有涉及到的物质是碱,故填:碱.
故答案为:
(1)O2;H2O; 灭火.
(2)Fe+CuSO4═FeSO4+Cu; CuO+H2SO4═CuSO4+H2O.(3)碱
点评 本题为框图式物质推断题,根据题干提供的信息找准解题的突破口,直接得出有关物质的化学式,然后推断得出其他物质的化学式.

| A. | -4 | B. | -2 | C. | +2 | D. | +4 |
【提出问题】刚出窑的“石灰”有那些成分?
【猜想】I.只有氧化钙
II.只有碳酸钙
III.既有氧化钙也有碳酸钙
【实验探究】
(1)甲同学从样品中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物.甲同学据此认为试管中的固体为碳酸钙,即猜想II成立.乙同学认为上述实验不足以证明猜想II成立,其理由是沉淀也可能是未溶解的氢氧化钙.
(2)乙同学从样品中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生.乙同学据此认为试管中的固体只有氧化钙,即猜想I成立.丙同学认为乙的实验不足以证明猜想I成立,理由是滴加的稀盐酸不足量.
(3)丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和稀盐酸证明了猜想III成立,请完成他的实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量剩余固体于试管中,加水振荡,过滤,取滤液滴加无色酚酞溶液 ②取滤渣滴加足量的稀盐酸 | 溶液变红色 有气泡产生 | 猜想 III成立 |
【猜想】猜想一:没有变质; 猜想二:部分变质; 猜想三:(1)全部变质.
【查阅资料】Na2CO3溶液呈碱性.
【进行实验】对猜想二进行验证.
| 实验步骤 | 实验现象 | 结论 |
| (2)取少许该溶液于试管中,滴 入适量的BaCl2(CaCl2、Ba(NO3)2)溶液. | (3)有白色沉淀 | 猜想二正确 |
| (4)静置上述溶液,取上层清液少许于另一支试管中,滴入几滴 酚酞溶液 | (5)溶液变红 |
【反思】氢氧化钠溶液必须密封保存.
(7)氢氧化钠溶液变质的原因CO2+2NaOH═Na2CO3+H2O(用化学方程表示).
| A. | 青蒿素属于有机高分子化合物 | |
| B. | 青蒿素是由碳、氢、氧三个元素组成的 | |
| C. | 青蒿素中碳、氢、氧元素的质量比为15:22:5 | |
| D. | 青蒿素的每个分子有42个原子构成 |
| A. | 油脂 | B. | 水 | C. | 蛋白质 | D. | 纤维素 |
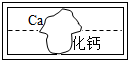 在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液,同学们对该实验进行了一系列的探究.
在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液,同学们对该实验进行了一系列的探究.探究一 M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M物质的溶质有两种可能:
①是氢氧化钙 ②是CaCl2.
【收集资料】CaCl2水溶液呈中性.
(2)【设计实验】同学们设计了如下方案并进行实验:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量M溶液于试管中,向其中滴加 酚酞 | 溶液变红 | 猜想①正确 |
【提出猜想】猜想一:NaOH 和Na2CO3; 猜想二:NaOH和Ca(OH)2;猜想三:NaOH.
(3)【实验验证】同学们针对“猜想一”进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入两滴稀盐酸 | 没有气体产生 | “猜想一”不成立 |
(4)【继续探究】设计实验方案确定滤液中溶质的组成.
| 实验操作 | 实验现象 | 实验结论 |
分别取少量滤液于A、B两支试管中,A中加入CaCl2溶液, B中加入Na2CO3溶液 | 若A中产生白色沉淀,B中没有沉淀 | “猜想一”成立 |
若A中没有沉淀,B中产生沉淀 | “猜想二”成立 | |
若AB中都没有沉淀 | “猜想三”成立 |