题目内容
6.将31g氯酸钾和二氧化锰的混合物进行加热,反应完全后,得到21.4g固体.求:(1)生成氧气的质量.
(2)原混合物中有多少克氯酸钾?
分析 氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,由质量守恒定律,固体混合物减少的质量即为生成氧气的质量,由氧气的质量、由反应的化学方程式列式计算出参加反应的氯酸钾的质量即可.
解答 解:(1)由质量守恒定律,生成氧气的质量为31g-21.4g=9.6g.
(2)参加反应的氯酸钾的质量为x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
x 9.6g
$\frac{245}{96}=\frac{x}{9.6g}$ x=24.5g
答:(1)设生成氧气的质量为9.6g;(2)原混合物中有24.5g氯酸钾.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出氧气的质量是正确解答本题的前提和关键.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案
相关题目
17. 小明同学看到妈妈将买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后迅速冒出气泡.为了解其反应过程,他与学习小组的同学进行了如下探究.
小明同学看到妈妈将买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后迅速冒出气泡.为了解其反应过程,他与学习小组的同学进行了如下探究.
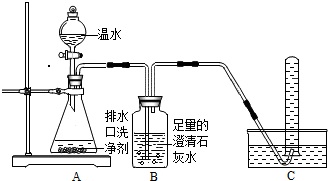
【探究一】小组同学根据所学的化学知识设计并进行了如图所示的实验.
要保证实验的效果,实验装置要有良好的气密性,检查A装置气密性的方法是关闭分液漏斗的活塞,将导气管一端浸没水中,手握锥形瓶的外壁,若导管口冒气泡,则气密性良好.
实验中观察到如下现象:A中有气泡产生;B中的澄清石灰水变浑浊;C中收集到的气体能使燃着的木条燃烧更旺.由此同学们得出结论:生成的两种气体分别是CO2、O2(填化学式).
【探究二】
(1)实验过程:教师提供了一瓶过碳酸钠(Na2CO4),小组同学进行了如下实验探究:
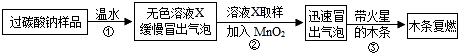
(2)提出问题:无色溶液X中的溶质有哪些物质?
(3)猜想与假设:根据以上实验现象,X溶液中一定存在的溶质是过氧化氢;还可能存在Na2CO3、NaHCO3、NaOH中的一种或几种.
写出上述实验探究中②反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(4)查找资料:
资料1:氯化钙溶液呈中性;氯化钙溶液与碳酸氢钠溶液混合不发生反应;
氯化钙溶液与碳酸钠溶液混合后发生如下反应:Na2CO3+CaCl2═CaCO3↓+2NaCl
资料2:NaHCO3溶液呈碱性,与石灰水反应生成白色沉淀;碳酸氢钠、碳酸钠与足量的酸反应产物相同.
(5)实验过程:小组同学对溶液X中的溶质进行了如下实验.请将下列实验方案填写完整.
(6)实验反思:①根据资料,NaHCO3溶液能与石灰水反应生成白色沉淀.于是,同学们猜想:碳酸氢钠与氢氧化钠是否反应?NaHCO3+NaOH=Na2CO3+H2O(如反应,请写出化学方程式,如不反应此空不填).②Na2CO3、NaHCO3两种物质性质上既有共性又有差异,其差异性可用于鉴别或分离或除杂等.
 小明同学看到妈妈将买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后迅速冒出气泡.为了解其反应过程,他与学习小组的同学进行了如下探究.
小明同学看到妈妈将买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后迅速冒出气泡.为了解其反应过程,他与学习小组的同学进行了如下探究.【探究一】小组同学根据所学的化学知识设计并进行了如图所示的实验.
要保证实验的效果,实验装置要有良好的气密性,检查A装置气密性的方法是关闭分液漏斗的活塞,将导气管一端浸没水中,手握锥形瓶的外壁,若导管口冒气泡,则气密性良好.
实验中观察到如下现象:A中有气泡产生;B中的澄清石灰水变浑浊;C中收集到的气体能使燃着的木条燃烧更旺.由此同学们得出结论:生成的两种气体分别是CO2、O2(填化学式).
【探究二】
(1)实验过程:教师提供了一瓶过碳酸钠(Na2CO4),小组同学进行了如下实验探究:

(2)提出问题:无色溶液X中的溶质有哪些物质?
(3)猜想与假设:根据以上实验现象,X溶液中一定存在的溶质是过氧化氢;还可能存在Na2CO3、NaHCO3、NaOH中的一种或几种.
写出上述实验探究中②反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(4)查找资料:
资料1:氯化钙溶液呈中性;氯化钙溶液与碳酸氢钠溶液混合不发生反应;
氯化钙溶液与碳酸钠溶液混合后发生如下反应:Na2CO3+CaCl2═CaCO3↓+2NaCl
资料2:NaHCO3溶液呈碱性,与石灰水反应生成白色沉淀;碳酸氢钠、碳酸钠与足量的酸反应产物相同.
(5)实验过程:小组同学对溶液X中的溶质进行了如下实验.请将下列实验方案填写完整.
| 实验操作 | 主要实验现象 | 结论 |
| ① | 证明溶液中有Na2CO3 | |
| ② | 证明溶液中既无NaHCO3又无NaOH |
4.下列变化中不属于化学变化的是( )
| A. | 用粮食酿制食醋 | B. | 风力发电 | ||
| C. | 从海水中提取金属镁 | D. | 铁制品生锈 |
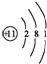
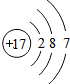
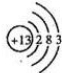
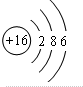 .
.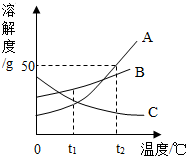 (1)目前属于最清洁的气体燃料是氢气;
(1)目前属于最清洁的气体燃料是氢气;