题目内容
3.请判断一下反应能否发生反应,若不能请说明理由,若能请写出化学方程式:(1)铝与硫酸铜溶液:2Al+3CuSO4═Al2(SO4)3+3Cu;
(2)氢氧化钠溶液与硫酸铜溶液:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;
(3)硝酸银溶液与氯化铜溶液:2AgNO3+CuCl2=2AgCl↓+Cu(NO3)2;
(4)氢氧化钠溶液与硫酸溶液:2NaOH+H2SO4=Na2SO4+2H2O.
分析 在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢;位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,发生复解反应能反应时,两种化合物相互交换成分必须生成沉淀、气体、水才能反应;据此判断能否发生反应,写出反应的化学方程式即可.
解答 解:(1)铝和硫酸铜反应生成硫酸铝和铜,化学方程式为:2Al+3CuSO4═Al2(SO4)3+3Cu;
(2)氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,化学方程式为:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;
(3)硝酸银和氯化铜反应生成硝酸铜和氯化银沉淀,化学方程式为:2AgNO3+CuCl2=2AgCl↓+Cu(NO3)2;
(4)氢氧化钠和硫酸反应生成硫酸钠和水,化学方程式为:2NaOH+H2SO4=Na2SO4+2H2O.
故答案为:(1)2Al+3CuSO4═Al2(SO4)3+3Cu;
(2)2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;
(3)2AgNO3+CuCl2=2AgCl↓+Cu(NO3)2;
(4)2NaOH+H2SO4=Na2SO4+2H2O.
点评 本题难度不大,考查了金属活动性顺序的应用,掌握金属活动性顺序、复解反应的条件,化学方程式的书写并能灵活运用是正确解答此类题的关键所在.

练习册系列答案
相关题目
5.小红发现,金店里有两种不同的“白金”,单价相差悬殊,小红很好奇,打算进行研究.
【查阅资料】市场上所谓的“白金”通常有两种,一种是金、镍、铜、锌的合金,称为白色金;另一种是铂金,铂是一种银白色的贵重金属,用于耐腐蚀的化学仪器及首饰等,俗称“白金”(元素符号Pt).小红结合化学课上学习的金属活动性顺序,展开了下列实验活动.
(1)鉴别两种白金,她的方法是取两种白金分别放入盛有稀盐酸的试管中,有气泡产生的是白色金,无气泡的是铂金;
(2)探究Zn、Ni(镍)、铜的活动性顺序.
【作出假设】对三种金属的活动性顺序提出可能的假设:①Zn>Ni>Cu;②Zn>Cu>Ni你觉得还有其他的可能性吗?请把它们写出来(一种即可)
假设:③Ni>Zn>Cu …
[查阅资料】小红同学查阅了部分含镍化合物的溶解性如下表,且得知镍能与酸反应.
【设计实验】同温下,取大小、厚度相同的这三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象.
【记录现象】请帮助小红把实验现象填写完整
【得出结论】原假设中正确的是①(填序号);写出镍与盐酸反应的化学方程式Ni+2HCl═NiCl2+H2↑.
【结论应用】
①根据探究结果,请你预测镍与硫酸铜溶液能(填“能”或“不能”)反应.
②除小红的实验设计外,你能否象小红一样,设计另一组实验,也这样一次验证上述假设的正确与否,小红同学小张的设计所用的一组物质的化学式是Zn、NiSO4溶液、Cu.
【查阅资料】市场上所谓的“白金”通常有两种,一种是金、镍、铜、锌的合金,称为白色金;另一种是铂金,铂是一种银白色的贵重金属,用于耐腐蚀的化学仪器及首饰等,俗称“白金”(元素符号Pt).小红结合化学课上学习的金属活动性顺序,展开了下列实验活动.
(1)鉴别两种白金,她的方法是取两种白金分别放入盛有稀盐酸的试管中,有气泡产生的是白色金,无气泡的是铂金;
(2)探究Zn、Ni(镍)、铜的活动性顺序.
【作出假设】对三种金属的活动性顺序提出可能的假设:①Zn>Ni>Cu;②Zn>Cu>Ni你觉得还有其他的可能性吗?请把它们写出来(一种即可)
假设:③Ni>Zn>Cu …
[查阅资料】小红同学查阅了部分含镍化合物的溶解性如下表,且得知镍能与酸反应.
| OH- | NO3- | SO42- | Cl- | |
| Ni2+ | 不 | 溶 | 溶 | 溶 |
【记录现象】请帮助小红把实验现象填写完整
| 金属 | Ni | Zn | Cu |
| 与盐酸反应的现象 | 气体产生缓慢 金属逐渐溶解 | 气体产生激烈 金属迅速溶解 | 无明显现象 |
【结论应用】
①根据探究结果,请你预测镍与硫酸铜溶液能(填“能”或“不能”)反应.
②除小红的实验设计外,你能否象小红一样,设计另一组实验,也这样一次验证上述假设的正确与否,小红同学小张的设计所用的一组物质的化学式是Zn、NiSO4溶液、Cu.
8.下列说法正确的是( )
①工业上采用分离液态空气的方法制备氧气和氮气
②氢气等可燃性气体在点燃前要检验气体的纯度
③一般情况下合金的熔点和硬度都比组成合金的纯金属高
④氢氧化钠固体潮解、变质与水蒸气和二氧化碳有关
⑤二氧化碳、二氧化硫、二氧化氮和一氧化碳都是大气污染物.
①工业上采用分离液态空气的方法制备氧气和氮气
②氢气等可燃性气体在点燃前要检验气体的纯度
③一般情况下合金的熔点和硬度都比组成合金的纯金属高
④氢氧化钠固体潮解、变质与水蒸气和二氧化碳有关
⑤二氧化碳、二氧化硫、二氧化氮和一氧化碳都是大气污染物.
| A. | ②③④ | B. | ①②④ | C. | ①③⑤ | D. | ③④⑤ |
15.“碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用.如可利用NaOH溶液来“捕捉”CO2,其基本过程如图所示(部分条件及物质未标出).
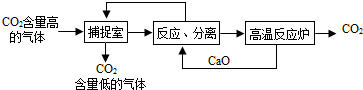
下列有关该方法的叙述中不正确的是( )

下列有关该方法的叙述中不正确的是( )
| A. | 能耗大是该方法的一大缺点 | |
| B. | 整个过程中,有两种物质可以循环利用 | |
| C. | “反应分离”环节中,分离物质的基本操作是蒸发结晶、过滤 | |
| D. | 该方法可减少碳排放,捕捉到的CO2还可用来制备甲醇(CH4O)等产品 |
13.下列实验操作正确的是( )
| A. | 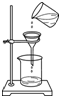 | B. | 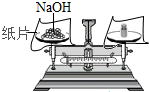 | C. |  | D. |  |