题目内容
17.托盘天平两边各放一只烧杯,分别注入等质量等质量分数的足量稀盐酸,调节至平衡,先向左烧杯中加入4.0g含钙元素50%的碳酸钙和氧化钙的固体混合物,再向右烧杯中加入一定质量的5%的硝酸银溶液,若充分反应后天平再次平衡,则右边烧杯中应该加入硝酸银溶液( )| A. | 2.24g | B. | 2.8g | C. | 2.9g | D. | 无法计算 |
分析 由于碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,氧化钙与盐酸反应生成氯化钙和水;所以左烧杯中增加的质量=4.0g-二氧化碳的质量;所以右边烧杯中应该增加相同的质量.
解答 解:设4.0g含钙元素50%的碳酸钙和氧化钙的质量分别为x,y
$\left\{\begin{array}{l}{\frac{x×\frac{40}{100}+y×\frac{40}{56}}{4.0g}×100%=50%}\\{x+y=4.0g}\end{array}\right.$
解得:x≈2.73g,y≈1.27g
设2.73g碳酸钙与盐酸反应生成二氧化碳的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
2.73g x
$\frac{100}{2.73g}=\frac{44}{x}$
x≈1.2g
所以左烧杯中增加的质量为4.0g-1.2g=2.8g
由于硝酸银与盐酸反应生成氯化银和硝酸,所以加入硝酸银溶液的质量即为增加的质量,所以右边烧杯中应该加入硝酸银溶液2.8g,
故选:B.
点评 本题较难,考查的内容较多,需要考虑多方面的知识,要运用多种方法计算.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案
相关题目
7.家庭用煤经过从“煤球”到“蜂窝煤”的变化,其目的是( )

| A. | 增大可燃物的热值 | B. | 降低可燃物的着火点 | ||
| C. | 提高空气中氧气的含量 | D. | 增大可燃物与空气的接触面积 |
8.二氧化硅是玻璃的主要成分,二氧化硅(SiO2)中硅元素的化合价的是( )
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
5.化学魔术“滴水生火”的操作是用棉花包住少量过氧化钠(Na2O2)粉末,放在石棉网上,向棉花上滴加几滴水,观察到棉花迅速燃烧.该反应的化学方程式为:2Na2O2+2H2O═4NaOH+X↑,下列推测不正确的是( )
| A. | 该反应可能放出大量的热 | B. | X的化学式为O2 | ||
| C. | 滴加少量水就可以灭火 | D. | 棉花是可燃物 |
12.下列人类活动一般不会对空气造成污染的是( )
| A. | 露天焚烧垃圾 | B. | 利用风能发电 | C. | 工厂排放烟尘 | D. | 汽车排放尾气 |
2.安徽的土特产品种类繁多,历史悠久,独具地方特色.下面是省内的著名土特产,其中所含营养物质维生素较多的是( )
| A. |  马鞍山采石茶干 | B. |  老任桥牛肉 | C. |  怀远石榴 | D. |  黄山烧饼 |
9.铬和钼两种金属在现代科技发展中有着非常重要的作用,可用于电镀和制造特种钢,下列有关说法错误的是( )
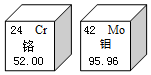

| A. | 在化学反应中,Cr原子和Mo原子都易失去电子 | |
| B. | 铬原子的质子数为24 | |
| C. | 铬原子的相对原子质量为52.00 | |
| D. | 钼离子的棱外电子数为42 |