题目内容
14.以化学方程式CH4+2O2$\underline{\underline{点燃}}$CO2+2H2O为例,写出能表示下面要求的读法.(1)宏观:甲烷在空气中点燃生成水和二氧化碳;
(2)微观:1个甲烷分子和2个氧分子在点燃的条件下生成1个二氧化碳分子和2个水分子;
(3)质量关系:16份质量的甲烷和64份质量的氧气在点燃的条件下生成44份质量的二氧化碳和36份质量的水.
分析 化学方程式可表示:反应物和生成物的种类;反应的条件;反应物和生成物的微观粒子个数比;反应物和生成物的质量比等.但要注意读化学方程式时,“+”应读作“和”,“═”应读作“生成”,据此进行分析解答.
解答 解:根据化学方程式CH4+2O2$\underline{\underline{点燃}}$CO2+2H2O;从宏观方面看:该反应的反应物是甲烷和氧气,生成物是二氧化碳和水;反应条件是点燃;从微观方面看:一个甲烷分子和二个氧分子在点燃的条件下生成一个二氧化碳分子和二个水分子;从质量方面看:每16份质量的甲烷和64份质量的氧气在点燃条件下恰好反应生成44份质量的二氧化碳和36份质量的水;
故答案为:(1)甲烷在空气中点燃生成水和二氧化碳;(2)1个甲烷分子和2个氧分子在点燃的条件下生成1个二氧化碳分子和2个水分子;(3)16份质量的甲烷和64份质量的氧气在点燃的条件下生成44份质量的二氧化碳和36份质量的水.
点评 本题难度不大,化学方程式是最重要的化学用语之一,掌握化学方程式的含义、了解化学方程式的读法是正确解答此类题的关键.

练习册系列答案
相关题目
5.如图基本操作中正确的是( )
| A. |  | B. | 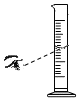 | C. | 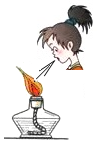 | D. | 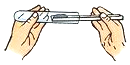 |
9.下列叙述中正确的是( )
| A. | 化石燃料作为重要的能源,对人类社会的发展百利无一害 | |
| B. | 可燃物在任何条件下燃烧都会发生爆炸 | |
| C. | 人类利用的能量都是通过化学反应获得的 | |
| D. | 选择燃料要综合考虑各种因素趋利避害 |
19.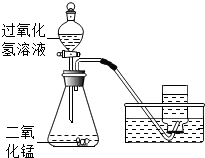 如图所示,实验室用过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如表:
如图所示,实验室用过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如表:
请回答:
(1)反应中二氧化锰的作用催化作用;
(2)反应生成氧气的质量为1.6g(计算结果精确至0.1g,下同);
(3)计算参加反应的过氧化氢的质量,写出计算过程.
 如图所示,实验室用过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如表:
如图所示,实验室用过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如表:| 气体发生装置内物质的总质量/g | |
| 反应前 | 38.2 |
| 反应后 | 36.6 |
(1)反应中二氧化锰的作用催化作用;
(2)反应生成氧气的质量为1.6g(计算结果精确至0.1g,下同);
(3)计算参加反应的过氧化氢的质量,写出计算过程.
3. 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
(1)请写出镁条与氧气反应的化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律.我不同意(“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
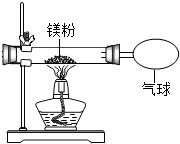
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
空气中N2的含量计远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,为什么呢?请给出合理的解释氧气的化学性质比氮气更活泼,镁条更容易与氧气发生反应.注意:若答对第(3)小题奖励4分,化学试卷总分不超过60分.
(4)该兴趣小组又做了镁条与盐溶液反应的实验,发现均能产生H2,实验现象如表:
如表中,用水进行实验的目的是对比.根据上表中的实验现象,请写出三条结论,并分析可能的原因(不分析原因,不得分):①盐可以做镁与水反应的催化剂,因为盐能加快产生气体的速率;②温度改变反应速率,因为升高温度可以加快产生气体的速率;③升高温度能使反应更复杂,因为升高温度使镁与水反应的生成物在与盐反应生成氨气(NH3).
 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.(1)请写出镁条与氧气反应的化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律.我不同意(“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
| 实验操作 | 实验现象及结论 |
| 将镁条燃烧的产物放在一只试管中,加入少量的蒸馏水,然后将一湿润的红色石蕊试纸放在试管口,观察现象 | 看到红色的石蕊试纸变成蓝色,说明黄色固体为氮化镁 |
(4)该兴趣小组又做了镁条与盐溶液反应的实验,发现均能产生H2,实验现象如表:
| 实验序号 | 实验1 | 实验2 | 实验3 | |
| 与镁条反应的溶液 | NH4Cl | NaCl | Na2SO4 | H2O |
| 实验现象 | 有大量气泡产生 | 有较多气泡产生 | 有少量气泡产生 | 气泡极少 |
| 加热后,实验现象 | 气泡明显增多可闻到氨味 | 气泡增多 | 气泡增多 | 气泡增多 |
20.某化学学习小组的同学围绕“澄清石灰水与碳酸钠溶液的反应”展开了如下探究活动.
(1)该反应的化学方程式为Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
(2)反应后溶液中的溶质是什么?同学们一致认为有以下三种情况:①②③
①氢氧化钠和氢氧化钙;②氢氧化钠和碳酸钠;③氢氧化钠.
(3)小新取少量溶液于试管中,滴加过量稀盐酸,发现无气泡产生,说明情况②(填序号)是不可能的.
为了进一步确定溶液的成分,同学们设计了如下实验方案:
小红选择了另外一种不同类别的物质CO2(填化学式),也得到了同样的结论.
在同学们的合作下,他们顺利完成了探究任务.
(1)该反应的化学方程式为Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
(2)反应后溶液中的溶质是什么?同学们一致认为有以下三种情况:①②③
①氢氧化钠和氢氧化钙;②氢氧化钠和碳酸钠;③氢氧化钠.
(3)小新取少量溶液于试管中,滴加过量稀盐酸,发现无气泡产生,说明情况②(填序号)是不可能的.
为了进一步确定溶液的成分,同学们设计了如下实验方案:
| 实验步骤 | 现象 | 结论 |
| 情况①正确 |
在同学们的合作下,他们顺利完成了探究任务.
