题目内容
5.某纯碱样品中含有少量氯化钠.为测定样品中碳酸钠的质量分数,现称取该样品11g,加入到盛有50g稀盐酸的烧杯中,恰好完全反应,最后称得烧杯中溶液的质量为56.6g.计算:(1)产生二氧化碳的质量是4.4g
(2)纯碱样品中碳酸钠的质量分数;
(3)反应后所得溶液中溶质的质量分数.
分析 反应前后的质量差即为反应生成二氧化碳的质量,根据二氧化碳的质量可以计算碳酸钠的质量和生成的氯化钠的质量,进一步可以计算纯碱样品中碳酸钠的质量分数和反应后所得溶液中溶质的质量分数.
解答 解:(1)生成二氧化碳的质量为:11g+50g-56.6g=4.4g,
故填:4.4.
(2)设碳酸钠的质量为x,生成氯化钠的质量为y,
Na2CO3+2HCl=2NaCl+H2O+CO2↑,
106 117 44
x y 4.4g
$\frac{106}{x}$=$\frac{117}{y}$=$\frac{44}{4.4g}$,
x=10.6g,y=11.7g,
纯碱样品中碳酸钠的质量分数为:$\frac{10.6g}{11g}$×100%=96.4%,
答:纯碱样品中碳酸钠的质量分数为96.4%.
(3)反应后所得溶液中溶质的质量分数为:$\frac{11g-10.6g+11.7g}{56.6g}$×100%=21.4%,
答:反应后所得溶液中溶质的质量分数为21.4%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
16.某化学兴趣小组的同学做了如图所示两个实验.
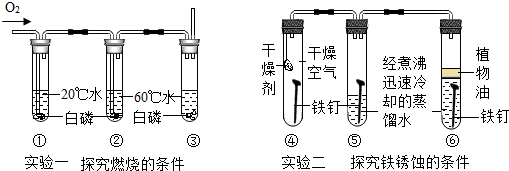
下列有关说法正确的是( )

下列有关说法正确的是( )
| A. | ①②号试管对比说明燃烧需要温度超过着火点 | |
| B. | 实验一、实验二所发生的反应都属于氧化反应,都发光放热 | |
| C. | ⑤、⑥号试管变量是水蒸气 | |
| D. | 实验二铁锈蚀也不能排除空气中二氧化碳参与反应的可能 |
13.下列是纯净物的是( )
| A. | 蒸馏水 | B. | 澄清的石灰水 | C. | 空气 | D. | 过氧化氢溶液 |
20.用50mL的量筒量取40mL水时,采用仰视的读法,则量取水的实际体积是( )
| A. | 大于40 mL | B. | 小于40 mL | C. | 40 mL | D. | 无法确定 |