题目内容
18.为研究氢氧化钠、氢氧化钙两种溶液的化学性质,进行如下实验.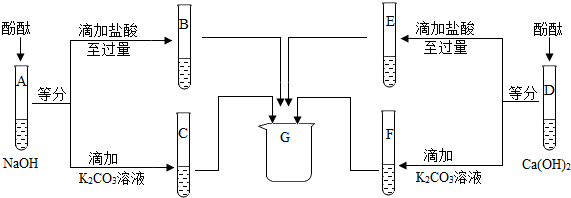
①A、D中酚酞均变红色,说明两种溶液都呈碱性.
②B中溶液的pH<7(选填“>”、“<”或“=”).写出氢氧化钠与盐酸反应的化学方程式HCl+NaOH═NaCl+H2O.
③F中沉淀的化学式是CaCO3.
④四支试管内的物质在G中混合后得到无色溶液,其中一定含有的溶质是氯化钠、氯化钙、氯化钾,可能含有的溶质是盐酸.
分析 ①根据碱溶液能使酚酞试液变成红色分析回答.
②根据酸性溶液的pH小于7,氢氧化钠能与盐酸发生中和反应分析回答.
③根据氢氧化钙能与碳酸钾反应生成了碳酸钙沉淀分析回答.
④根据四支试管内的物质在G中混合后得到无色溶液,说明了溶液呈酸性或中性,不存在氢氧化钠、碳酸钠和碳酸钾,据此分析一定存在的物质和可能存在的物质.
解答 解:①A、D中酚酞均变红色,说明两种溶液都呈碱性.
②由实验的过程可知,B溶液中有过量的盐酸,显酸性,溶液的pH<7.氢氧化钠与盐酸反应生成氯化钠和水,反应的化学方程式为:HCl+NaOH═NaCl+H2O.
③F中的沉淀是氢氧化钙与碳酸钾反应的碳酸钙,化学式是:CaCO3.
④由题意可知,四支试管内的物质在G中混合后得到无色溶液,说明了溶液呈酸性或中性,不存在氢氧化钠、氢氧化钙和碳酸钾.混合时过量的盐酸能与氢氧化钠、碳酸钾、氢氧化钾、碳酸钙反应,所以反应的溶液中一定含有的溶质是:氯化钠、氯化钙、氯化钾,可能含有的溶质是盐酸.
故答为:①红. ②<,HCl+NaOH═NaCl+H2O.③CaCO3.④氯化钠、氯化钙、氯化钾,盐酸.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.诗词是中华民族灿烂文化的瑰宝,下列诗句描述中只涉及物理变化的是( )
| A. | 爆竹声中一岁除,春风送暖入屠苏 | B. | 千里冰封,万里雪飘 | ||
| C. | 千锤万凿出深山,烈火焚烧若等闲 | D. | 春蚕到死丝方尽,蜡炬成灰泪始干 |
13.已知磷原子的核电荷数是15,相对原子质量是31,则磷原子的核内质子数是( )
| A. | 15 | B. | 16 | C. | 31 | D. | 46 |
3.“关注西部学生小餐桌”计划已经正式启动,用于改善贫困地区的中小学生营养状况.我市某中学制定出星期五的学生食谱:
则用你所学的知识.建议该校厨房增加的食物是( )
| 主食 | 米饭 |
| 副食 | 炒牛肉 |
| 饮料 | 酸牛奶、白开水 |
| A. | 炒白菜 | B. | 淸蒸鲫鱼 | C. | 炖豆腐 | D. | 水煮鸡蛋 |
10.如图是元素周期表中硅元素的信息示意图,对图中信息解释不正确的是( )


| A. | 原子序数为14 | B. | 质子数为14 | ||
| C. | 原子质量为28.09g | D. | 属于非金属元素 |
 贺州市矿产资源非常丰富,其中有色金属矿产有锡、钨、铅、锌、铜、锑等;化工原料矿产有赤铁矿、硫铁矿(主要成分:FeS2)等;建筑材料有大理石、花岗石、石灰石等.
贺州市矿产资源非常丰富,其中有色金属矿产有锡、钨、铅、锌、铜、锑等;化工原料矿产有赤铁矿、硫铁矿(主要成分:FeS2)等;建筑材料有大理石、花岗石、石灰石等. 为了测定生铁中铁的质量分数,某校化学兴趣小组进行了实验研究,取6g生铁与溶质的质量分数为14.6%的盐酸反应(生铁中杂质不溶于水,也不与盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图.
为了测定生铁中铁的质量分数,某校化学兴趣小组进行了实验研究,取6g生铁与溶质的质量分数为14.6%的盐酸反应(生铁中杂质不溶于水,也不与盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图.