题目内容
18.关于水的电解实验,下列说法正确的是( )| A. | 实验证明水是一种混合物 | |
| B. | 水电解的时间要略长,否则氧气会因为太少很难燃烧起来 | |
| C. | 在水通直流电后,在正极产生体积较大的气体 | |
| D. | 这个实验证明了水是由氧元素和氢元素组成的 |
分析 根据电解水的实验现象、结论和生成气体的性质分析判断,电解水时“正氧负氢、氢二氧一”.
解答 解:A、实验证明水是由氢、氧两种元素组成的化合物,不是混合物,故A错误;
B、氧气具有助燃性,不具有可燃性,故B错误;
C、在水通直流电后,在正极产生体积较少的气体,是氧气;故C错误;
D、这个实验证明了水是由氧元素和氢元素组成的,故D正确.
故选D.
点评 本题较为简单,了解了电解水的实验现象、结论和生成气体的性质即可分析判断.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
8.继黄金、白金之后,钯金(Pd)首饰在市场上悄然兴起,为了获得钯金,取17.7%的PdCl2溶液100g,加入10.0g铁粉使其充分反应得到钯金和铁的氧化物,经分析所得钯金的质量为10.6g.未反应的铁粉质量为4.4g,下列说法正确的是( )
| A. | 生成铁的氯化物质量为12.7g | B. | 生成铁的氯化物质量为16.25g | ||
| C. | 生成铁的氯化物为FeCl2和FeCl3 | D. | 生成铁的氯化物为FeCl3 |
9.建立一个适当的模型来反映和代替客观对象,可以帮助我们认识和理解观察不到的化学反应.如图为某反应的部分微观示意图,其中不同的球代表不同元素的原子.下列说法正确的是( )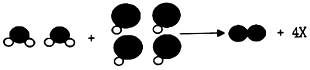
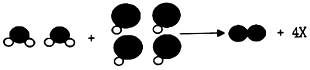
| A. | 该反应属于化合反应 | |
| B. | 黑球表示的元素的化合价在反应前后未改变 | |
| C. | 1个X分子中含有3个原子 | |
| D. | 参加反应的两种分子个数比为1:1 |
6.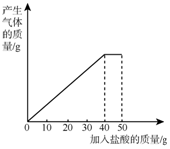 石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象.
石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象.
请计算:
(1)由图象可知,第四次加入10g盐酸后,碳酸钙固体又反应掉4克.
(2)完全反应后产生的二氧化碳.
(3)所加盐酸的溶质质量分数.
 石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象.
石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象.| 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 10 | 10 | 10 |
| 剩余固体的质量/g | 16 | 12 | 8 |
(1)由图象可知,第四次加入10g盐酸后,碳酸钙固体又反应掉4克.
(2)完全反应后产生的二氧化碳.
(3)所加盐酸的溶质质量分数.
13.甲、乙两同学在室温下各取50克某溶液分别做制晶体实验,甲将溶液蒸发掉10克水后冷却至室温得晶体4克(晶体不含结晶水),乙将溶液蒸发掉15克水后冷却至室温,得晶体9克.若两人实验结果都正确,则某溶液中溶质的质量分数为( )
| A. | 28.6% | B. | 37.5% | C. | 40% | D. | 44% |
10.溶液与人类生活息息相关,溶液的配制是日常生活和科学实验中常见的操作.下表是硫酸液和氨水的密度与其溶质质量分数对照表(20°C).请你仔细分析后回答下列问题:
(1)在20°C时,随着溶液中溶质质量分数的逐渐增大,氨水的密度逐渐减小.
(2)配制溶质质量分数4%的硫酸溶液50毫升,需要溶质质量分数24%的硫酸溶液多少毫升?水多少毫升?
| 溶液中溶质的质量分数 | 4% | 12% | 16% | 24% | 28% |
| 硫酸溶液的密度(g/cm3) | 1.02 | 1.08 | 1.11 | 1.17 | 1.20 |
| 氨水的密度(g/cm3) | 0.98 | 0.95 | 0.94 | 0.91 | 0.90 |
(2)配制溶质质量分数4%的硫酸溶液50毫升,需要溶质质量分数24%的硫酸溶液多少毫升?水多少毫升?
8.下列物质的化学式与名称表示一致并且书写正确的是( )
| A. | NH4HCO3--碳酸氢氧 | B. | CaO--熟石灰 | ||
| C. | NaOH--纯碱 | D. | CO(NH2)2--尿素 |