题目内容
11.下列试剂中,应该用药匙取用的是(1)(3),应该用镊子取用的是(2),应该用滴管取用的是(4)(1)氧化铜粉末
(2)石灰石块
(3)小颗粒锌粒
(4)试剂瓶中的稀盐酸.
分析 了解常用仪器的作用,药匙用来取用粉末状固体药品;镊子用来取用固体药品;滴管可用来吸取液体药品.
解答 解:氧化铜粉末是粉末状的固体药品,可用药匙取用;石灰石块是固体药品,要用镊子取用;小颗粒锌粒,可用药匙取用;试剂瓶中的盐酸是液体药品,可用滴管取用;故答案为:(1)(3)、(2)、(4).
点评 本题考查常见仪器的作用,要求同学们在平时的实验中多加留心各种实验仪器的作用.

练习册系列答案
相关题目
1.下列各组化合物含有同种原子团的是( )
| A. | Na2SO4和Na2SO3 | B. | Na2CO3和NaHCO3 | C. | KNO2和KMnO4 | D. | AgNO3和NH4NO3 |
2.60g溶质质量分数为10%的硝酸钠溶液,欲将其溶质质量分数增加一倍,应该采取的方法是( )
| A. | 把溶剂蒸发掉$\frac{1}{2}$ | B. | 加入7.5g硝酸钠固体 | ||
| C. | 把溶剂蒸发掉30g | D. | 加入20%的硝酸钠溶液30g |
19.奠定近代化学基础的是( )
| A. | 原子论和分子学说 | B. | 火的发现和利用 | ||
| C. | 门捷列夫元素周期律的发现 | D. | 纳米技术的出现和利用 |
16.以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(常温通常指20℃;“浓度”指溶质的质量分数)
(1)通过实验①和②对比可知,化学反应快慢与过氧化氢的浓度有关;
(2)通过对比实验③和④可知,化学反应快慢与温度的关系是温度越高反应速度越快,温度越低反应速度越慢.
(3)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是20℃时5%过氧化氢溶液中加入少量二氧化锰.
(4)为什么过氧化氢分解制氧气一开始反应很快,过一段时间后反应又很慢.过氧化氢浓度降低,浓度低反应速率减慢.
| 实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液质量/g | 温度/℃ | 二氧化锰用量/g | 氧气体积/mL | 反应所需时间/s |
| ① | 5 | 12 | 20 | 0.2 | 125 | 11 |
| ② | 30 | 12 | 20 | 0.2 | 125 | 2 |
| ③ | 30 | 12 | 40 | / | 125 | 148 |
| ④ | 30 | 12 | 90 | / | 125 | 82 |
(2)通过对比实验③和④可知,化学反应快慢与温度的关系是温度越高反应速度越快,温度越低反应速度越慢.
(3)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是20℃时5%过氧化氢溶液中加入少量二氧化锰.
(4)为什么过氧化氢分解制氧气一开始反应很快,过一段时间后反应又很慢.过氧化氢浓度降低,浓度低反应速率减慢.
20.下列实验基本操作正确的是( )
| A. | 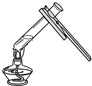 液体的加热 | B. | 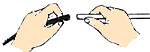 玻璃管套上橡皮管 | ||
| C. | 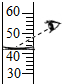 读取液体体积 | D. | 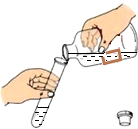 液体的倾倒 |